以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
| 难溶物 |
Ksp |
| Ca3(AsO4)2 |
6.8× 10-19 10-19 |
| AlAsO4 |
1.6×1 0-16 0-16 |
| FeAsO4 |
5.7×10-21 |
| 污染物 |
H2SO4 |
As |
| 浓度 |
28.42 g/L |
1.6 g·L-1 |
| 排放标准 |
pH 6~9 |
0.5 mg·L-1 |
表1.几种砷酸盐的Ksp 表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= ▲ mol·L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]= ▲ ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO43-)的最大是 ▲ mol·L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 ▲ 。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ▲ ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 ▲ 。
感冒是一种常见的病,人患了感冒会咳嗽、流涕、发烧,多喝开水多休息,适当服用一些治疗感冒的药,可以舒缓症状,减轻病情。
(1)药物阿司匹林是一种传统的治疗感冒发烧的老药,从分子结构上看,它可以看作是乙酸酯,其结构简式如下图: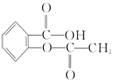
作为一种解热镇痛药,对于感冒发烧,它有较好的疗效,但大剂量长期空腹服用,容易对胃肠道产生刺激,原因是阿司匹林在胃中会发生酯的水解反应,生成_________和_________(用结构简式表示),阿司匹林分子水解后,能电离出氢离子(H + )的官能团增多,增大了对胃肠道的刺激。
(2)为减小副作用,一般宜饭后服药,并同时服用少量辅助药物,在①硫酸镁、②氢氧化钡、③碳酸钙中选取哪一种?
某同学欲检验抗酸药中是否含有Al(OH)3,操作如下:取药剂3~4片研碎,向样品中加入过量的盐酸,过滤,得澄清溶液,向澄清溶液中滴加NaOH溶液,观察到有白色沉淀,继续加过量NaOH溶液,白色沉淀又溶解。你能得出该抗酸药中__________(填“含”或“不含”)有Al(OH)3,请写出有关反应的化学方程式:
(1)_________________________________________________________________________;
(2)_________________________________________________________________________;
(3)_________________________________________________________________________。
下表是某食品包装袋上的说明:
| 品名 |
浓缩菠萝汁 |
| 配料 |
水、浓缩菠萝汁、蔗糖、柠檬酸、黄原胶、甜蜜素、维生素C、菠萝香精、柠檬黄、日落黄、山梨酸钾等 |
| 果汁含量 |
≥80% |
| 生产日期 |
标于包装袋封口上 |
从表中的配料中分别选出一种物质填在相应的横线上。其中属于着色剂的有__________,属于调味剂的有__________,属于调味剂的有__________,属于营养强化剂的有__________。
铁路提速为鲜活水产品、新鲜水果和蔬菜的运输提供了有利条件。在鲜活鱼的长途运输中,必须考虑以下几点:水中需要保持适量的O 2 ;及时除去鱼排出的CO 2 ;防止细菌的大量繁殖。现有两种在水中能起供氧灭菌作用的物质,其性质如下:
过氧化钠(Na2O2):易溶于水,与水反应生成NaOH和O2;
过氧化钙(CaO2):微溶于水,与水反应生成Ca(OH)2和O2。
根据以上介绍,你认为运输鲜活水产品时选择哪种物质加入水中更好?原因是___________________________________________________。
聚苯乙烯快餐盒、一次性塑料包装袋和聚氯乙烯农用地膜被视为危害环境的三大“白色公害”。为解决一次性快餐盒所带来的“白色污染”问题,国家已于2000年11月禁止使用泡沫塑料饭盒,取而代之的是用纸浆、植物纤维等易循环利用原料制成的一次性“纸饭盒”。据报道,德国Danone公司现已开发出的六十天能自行降解的绿色食品盒(杯)——聚乳酸(分子式为C 3n H 4n+2 O 2n+1 ,分子结构中含有支链)包装材料。为解决农用地膜所带来的“白色污染”问题,我国武汉大学张俐娜教授提出了“以甘渣浆、麦秆、芦苇浆”为原料来生产“再生纤维素共混膜”的研究课题,已获成功。使用“共混膜”不但能使农作物增产20%,而且使用到最后,其成分的30%可被微生物吃掉,剩余部分也会在40天内自动降解,对土壤无副作用。请完成下列问题:
(1)人为因素引起的环境问题主要有两大类:一是生态破坏;二是_______。
| A.环境污染 | B.水土流失 |
| C.土地沙漠化 | D.水质差,缺水 |
(2)环保专家预言,废弃的地膜最终将成为祸害,你认为会造成什么祸害?
(3)有人建议焚烧处理这些一次性快餐盒和农用地膜等普通塑料废弃物,你认为是否可行?为什么?
(4)张俐娜教授的研究课题有什么积极的环保意义?
(5)德国公司生产的绿色食品杯所用的原料乳酸可以从甜菜发酵的糖液中提取,然后通过_______反应可生成聚乳酸。聚乳酸的降解可分为两个阶段:首先是纯化学反应水解成乳酸单体,然后是乳酸单体在微菌的高温下分解生成二氧化碳和水。这两步反应的化学方程式为___________________,___________________。