下列反应的离子方程式书写正确的是
| A.硫酸铝溶液中加入过量氨水 Al3++3OH- = Al(OH)3¯ |
B.电解饱和食盐水 2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| C.钠与水的反应 Na+2H2O = Na++2OH- +H2↑ |
D.单质铜与稀硝酸反应 Cu + 2H++ 2NO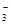 = Cu2+ + 2NO↑+H2O = Cu2+ + 2NO↑+H2O |
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列是有说法中,不正确的是( )
| A.1molNH5中含有5NA个N—H键(NA表示阿伏加德罗常数) |
B.NH5中既有共价键又有离子键 H H |
| C.NH5的电子式为:[H:N:H]+[:H]- H |
| D.它与水的反应的离子方程式为:NH4++H-+H2O=NH3·H2O+H2↑ |
(2008·信宜)根据等电子原理:由短周期元素组成的微粒,只要其原子数相同,各微粒的电子总数相同,则互称为等电子体。以下各组微粒不是等电子体的是( )
| A.CO和N2 | B.O3和NO2- | C.N2H4和C2H4 | D.CO2和 N2O |
现有aA、bB、cC、dD、eE五种短周期元素,它们都是生物体不可缺少的重要元素。已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e,B、D、E都有多种同素异形体。人类已知的化合物中,有一类化合物的种类已超过三千万种,这类化合物中一般都含有A、B两种元素。根据以上信息回答下列有关问题:
(1)请写出下列元素的元素符号: B_____________ D____________ E___________。
(2)写出B、D两元素组成的非极性分子的电子式___________________。
(3)写出由上述五种元素中的四种元素组成的离子化合物的化学式(写出2种即可)
_______________________________、________________________________。
(4)在A、B、D三种元素中选择2种或3种元素,组成2种可发生反应的阴离子,请写出该反应的离子方程式:_________________________________________。
(2008·武汉)下列各组物质中,将前者加入后者时,无论前者过量与否,都能用同一个化学方程式表示的是()
| A.澄清石灰水,CO2 | B.氢氧化钠溶液,AlCl3溶液 |
| C.Fe ,Cl2 | D.稀硫酸溶液,NaAlO2溶液 |
下列化学用语表达正确的是()
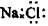 |
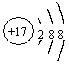
| A.S2-的结构示意图: | B.NaCl的电子式: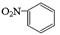 |
| C.乙炔的结构简式CHCH | D.硝基苯的结构简式: |