某原电池构造如图所示。下列有关叙述正确的是
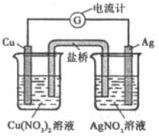
| A.在外电路中,电子由银电极流向铜电极 |
| B.取出盐桥后,电流计的指针仍发生偏转 |
| C.外电路中每通过0.1mol电子,铜的质量理论上减小6.4g |
| D.原电池的总反应式为Cu+2AgNO3=2Ag+Cu(NO3)2 |
向100mL pH=0的硫酸和硝酸混合溶液中投入3.84g铜粉,微热使反应充分完成后,生成NO气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为( )
| A.0.02mol | B.0.08mol | C.0.10mol | D.0.16mol |
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是()
| A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B.28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
| C.常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6 NA |
| D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA |
M、N、X、Y四种物质有如下转化关系(反应条件和其他产物已省略),下列选项不可能的是( )
| A.M:Na X:O2 |
| B.M:HNO3 X:Fe |
| C.M:Al X:NaOH |
| D.M:NH3 X:O2 |
在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w= ×100% ×100% |
B.溶质的物质的量浓度c= mol·L-1 mol·L-1 |
C.溶液中c(OH-)= mol·L-1 mol·L-1 |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
下列物质与其用途完全符合的有()条
①Na2CO3—制玻璃;②SiO2—太阳能电池;③AgI—人工降雨;④NaCl—制纯碱;
⑤Al2O3—焊接钢轨;⑥NaClO—消毒剂⑦Fe2O3—红色油漆或涂料 ⑧MgO—耐火材料
| A.4 | B.5 | C.6 | D.7 |