接触法制硫酸,接触室中反应为:2SO2+O2  2SO3 。对该反应的有关说法错误的是
2SO3 。对该反应的有关说法错误的是
| A.该反应是可逆反应 | B.反应中SO2能全部转化为SO3 |
| C.催化剂能加快该反应的速率 | D.升高温度能加快该反应的速率 |
3甲基戊烷的一氯代物有(不考虑立体异构)( )
| A.3种 | B.4种 | C.5种 | D.6种 |
下列叙述正确的是( )
| A.所有卤代烃都难溶于水,且都是密度比水大的液体 |
| B.卤代烃不属于烃类 |
| C.所有卤代烃都是通过取代反应制得 |
| D.卤代烃都是良好的有机溶剂 |
冰箱制冷剂氟氯甲烷在高空受紫外线辐射时产生Cl·原子,并能发生下列反应:Cl·+O3―→ClO·+O2,ClO·+O·―→Cl·+O2。下列说法不正确的是( )
| A.反应过程中将O3转变为O2 |
| B.Cl·是总反应的催化剂 |
| C.氟氯甲烷是总反应的催化剂 |
| D.Cl·起分解O3的作用 |
以溴乙烷为原料制取1,2二溴乙烷,下列转化方案中最好的是( )
A.CH3CH2Br  |
B.CH3CH2Br CH2BrCH2Br CH2BrCH2Br |
C.CH3CH2Br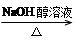 CH2===CH2 CH2===CH2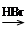 CH2BrCH3 CH2BrCH3 CH2BrCH2Br CH2BrCH2Br |
D.CH3CH2Br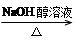 CH2===CH2 CH2===CH2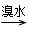 CH2BrCH2Br CH2BrCH2Br |
下列分子式中只表示一种纯净物的是( )
| A.C2H4Cl2 | B.C2H3Cl3 | C.C2HCl3 | D.C2H2Cl2 |