下图是日常生活中常见电动自行车主要部件之铅蓄电池结构示意图,有关说法不正确的是
| A.铅蓄电池属于二次电池 | B.实际使用过程中可以无限次充放电 |
| C.使用过程中负极发生氧化反应 | D.铅蓄电池体积大有污染还不是最理想的电池 |
过量的NaHCO3和Na2O2混合,在密闭容器中充分混合加热后,最后排出气体,残留的固体是( )
| A.Na2O | B.Na2CO3 |
| C.Na2O2和Na2CO3 | D.Na2O2和Na2O |
下列关于实验操作或说法正确的是( )
| A.从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶 |
| B.钠长期露置在空气中,最终产物是Na2CO3 |
| C.以蒸发溶剂的方法,除去酒精溶液中少量的水分 |
| D.用托盘天平称量25.20 g NaCl |
下列对物质用途的描述中,错误的是()
| A.碳酸钠在医疗上是治疗胃酸过多的一种药剂 |
| B.碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一 |
| C.氟化钠可用于预防龋齿 |
| D.钠的还原性很强,可以用来冶炼金属钛、锆、铌等 |
下列装置图中,中间的试管收集浓硝酸与铜丝反应所生成的气体,何者可使收集到的气体中空气的含量最少( )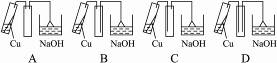
0.03 mol Cu完全溶于硝酸,产生氮的氧化物(NO、NO2、N2O4)混合气体共0.05 mol。该混合气体的平均相对分子质量可能是( )
| A.30 |
| B.46 |
| C.50 |
| D.66 |