某同学准备用下图所示装置制取H2还原氧化铜,在实验中发现稀硫酸不足,与锌粒无法接触而又无其他酸液可加入,经思考后他从长颈漏斗中加入适量的合适试剂完成了实验,下列试剂中不合适的是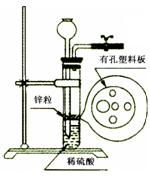
| A.苯 | B. 四氯化碳 |
C.酒精 | D.KCl溶液 |
将石墨置于熔融的钾或气态钾中,石墨会吸收钾而形成称为钾石墨的物质,其组成是 C8K、C24K、C36K、C48K和C60K。在钾石墨中,钾原子把价电子交给石墨层,但在遇到与金属钾易反应的其他物质时还会收回。在钾石墨中,钾元素处于石墨层中间,因而石墨层之间被胀大,层间的距离增加。下列对钾石墨的叙述中正确的是()
| A.钾石墨是一类高分子化合物 | B.钾石墨导电性比石墨强 |
| C.钾石墨与水相遇不发生任何反应 | D.题干所举出的5种钾石墨属于同素异形体 |
右图中曲线表示原子序数在前20号中的某些元素的原子序数(按递增顺序连续排列)和单质沸点的关系,其中A点表示的元素是( ) 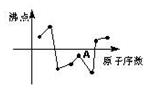
| A.Si | B.Al | C.F | D.S |
中子俘获治疗癌症(缩写为NCT)是一种新的化疗方法,化疗时用到的药物BSH,合成时必须经过中间体Na2B12H12,它可由B2H6和NaBH4以二甘二甲醚为溶剂,在180℃时合成的。已知B12H122-结构如右图。有关B12H122-的说法不正确的是()
| A.该粒子中硼原子构成20个正三角形 |
| B.一个B12H122-中含有30个硼硼键 |
| C.Na2B12H12属共价化合物 |
D.合成Na2B12H12反应可表示为: 5B2H6+2NaBH4  Na2B12H12+13H2 Na2B12H12+13H2 |
178O和 O原子的核外电子数( )
O原子的核外电子数( )
| A.大于 | B.小于 | C.等于 | D.不能肯定 |
H-H和H-F的键能 ( )
| A.大于 | B.小于 | C.等于 | D.不能肯定 |