用草酸的稀溶液或草酸钠的酸性溶液可以洗涤粘在皮肤上的高锰酸钾,其离子方程式为(未配平):MnO4-+C2O42-+H+ →CO2↑+Mn2++□。关于此反应的叙述正确的是
| A.该反应右边方框内的产物是OH- |
| B.配平该反应后,H+的化学计量数是8 |
| C.该反应中氧化产物是CO2 |
| D.该反应电子转移总数是5e- |
下列说法不正确的是()
| A.反应是放热还是吸热必须看生成物和反应物所具有的总能量的相对大小 |
| B.绿色植物进行光合作用时,将太阳能转化为化学能储存起来 |
| C.吸热反应中由于反应物总能量小于生成物总能量,因而无利用价值 |
| D.物质的化学能可以在一定条件下转化为热能、电能为人类所利用 |
已知室温时,0.1 mol·L–1某一元敌HA在水中有0.1%发生电离,下列叙述错误的是
| A.该溶液的pH=4 |
| B.升高温度,溶液的pH增大 |
| C.此酸的电离平衡常数为l×10–7 mol·L–1 |
| D.HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列措施不符合节能减排的是()
| A.大力发展火力发电,解决电力紧张问题 |
| B.发展低碳经济、循环经济,推广利用太阳能、风能 |
| C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏 |
| D.用杂草、生活垃圾及有机废弃物在沼气池中发酵产生沼气,作家庭燃气 |
下列物质的水溶液能导电,且属于非电解质的是()
| A.酒清 | B.Cl2 | C.NH4 NO3 | D.SO2 |
下列与金属腐蚀有关的说法正确的是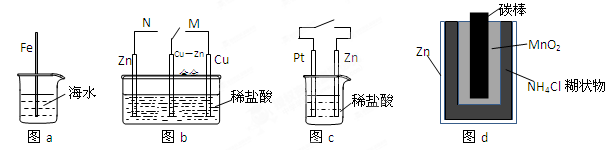
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |