关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是
| A.取等体积的两种酸溶液分别进行稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n |
| B.取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸 |
| C.取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多 |
| D.两种酸溶液中c(CH3COO-)=c(Cl-) |
将等体积的苯、汽油和水在试管中充分混合后静置。下列图示现象正确的是
下列化学用语书写正确的是
| A.乙醇的分子式:CH3CH2OH | B.丙烯的键线式: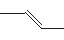 |
| C.乙烯的结构简式:CH2CH2 | D.甲烷的电子式: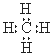 |
下列制取中,不需要加入碎瓷片的是()
| A.制乙烯 | B.制蒸馏水 | C.制溴苯 | D.石油分馏 |
氯化碘(ICl)的化学性质跟Cl2相似,预计它与H2O反应的最初生成物是
| A.HI和HClO | B.HCl和HIO | C.HClO3和HIO | D.HCl和HI |
有关键能数据如表:
| 化学键 |
Si—O |
O=O |
Si—Si |
| 键能kJ·mol-1 |
X |
498、8 |
176 |
晶体硅在氧气中燃烧的热化学方程式:Si(s)+O2(g)═SiO2(s)△H= —989、2 kJ·mol-1,则表中X的值为( )
A、423、3 B、460 C、920 D、1165、2