已知H2B在溶液中的电离方程式:H2B = H++HB-, HB- H++B2-。下列叙述一定正确的是
H++B2-。下列叙述一定正确的是
A. Na2B溶液存在:c (Na+) =" 2c" (HB-) + 2c(B2-) + 2c(H2B)
B.NaHB溶液一定显酸性
C.HB-的水解方程式:HB-+H2O H2B+OH-
H2B+OH-
D.NaHB溶液与稀盐酸反应的离子方程式是:HB-+H+ = H2B
用玻璃棒迅速搅拌如图所示装置内(小烧杯与玻璃片之间有一薄层水)的固体混合物。稍后手拿起烧杯时发现玻璃片与烧杯粘结在一起。下列有关该反应的说法中正确的是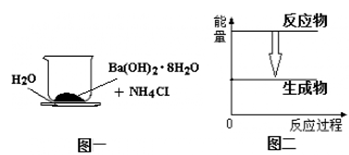
| A.反应中有化学能转化为热能 | B.反应中的能量关系如图二 |
| C.是吸热反应 | D.化学键的总键能:反应物<生成物 |
未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生。下列能源符合未来新能源标准的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
| A.①②③④ | B.⑤⑥⑦⑧ |
| C.③⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |
第3周期元素的基态原子中,不可能出现d电子,主要依据是
| A.能量守恒原理 |
| B.泡利不相容原理 |
| C.洪特规则 |
| D.近似能级图中的顺序3d轨道能量比4s轨道高 |
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,下列关于X、Y、Z、W四种元素的描述,不正确的是
| A.原子半径:X>Y>W>Z |
| B.原子序数:Y>X>Z>W |
| C.原子最外层电子数:Z>W>Y>X |
| D.离子半径:X+>Y2+>W2->Z- |
下列离子方程式中书写正确的是
| A.氯化铝溶液中加入足量的氨水:Al3++3NH3·H2O= Al(OH)3 ↓+3NH4+ |
| B.水玻璃中加入稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ |
| C.二氧化硅与苛性钠溶液反应:SiO2+OH-=SiO32-+H2O |
| D.氧化铝与NaOH溶液反应:Al2O3+10OH-= 2[Al(OH)4]-+H2↑ |