关于Na2CO3和NaHCO3比较中,下列说法不正确的是
| A.NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解 |
| B.等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多 |
| C.等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深 |
| D.Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同 |
下列溶液一定呈中性的是()
| A.pH=7的溶液 | B.c(H+)=c(OH-)=10-6mol/L溶液 |
| C.使石蕊试液呈紫色的溶液 | D.酸与碱恰好完全反应生成正盐的溶液 |
下列溶液中导电性最强的是()
A. 醋酸 醋酸 |
B.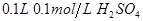 溶液 溶液 |
C.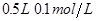 盐酸 盐酸 |
D. 溶液 溶液 |
某酸溶液中C(H+)=0.1mol·L-1,则该酸溶液的物质的量浓度()
| A.一定等于0.1mol·L-1 | B.一定大于0.1mol·L-1 |
| C.一定小于0.1mol·L-1 | D.无法确定 |
下列对于化学反应的认识正确的是()
| A.有气体生成的复分解反应能自发进行 |
| B.有热量放出的反应一定能自发进行 |
| C.需要吸收热量的过程不能自发进行 |
| D.凡是熵增加的反应一定能自发进行 |
在等体积的NaC1、MgCl2、A1Cl3三种溶液中,分别加入等体积且等物质的量量浓度的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为
| A.1:2:3 | B.3:2:1 | C.1:1:1 | D.6:3:2 |