镁电池毒性低、污染小,电压高而平稳,它逐渐成为人们研制绿色电池的关注焦点。其中一种镁电池的反应原理为: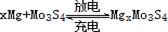 。下列说法不正确的是
。下列说法不正确的是
| A.放电时,Mo3S4发生氧化反应 |
| B.放电时,正极反应式:Mo3S4+2xe-→Mo3S42x- |
| C.充电时,Mg2+向阴极迁移 |
| D.充电时,阴极反应式:xMg2++2xe-→xMg |
等质量的下列有机物完全燃烧,消耗O2最多的是( )
| A.CH4 | B.CH2= CH2 | C. |
D.CH3CH2OH |
C6H12和C2H6O的混合物中氧的质量分数为8﹪,则混合物中氢的质量分数为( )
| A.8﹪ | B.13﹪ | C.14﹪ | D.78﹪ |
分子式为CH2Cl2的有机物同分异构体共有(不考虑立体异构)( )
| A.1种 | B.2种 | C.3种 | D.4种 |
在恒温恒容条件下,能使A(g)+B(g)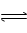 C(g)+D(g)正反应速率增大的措施是 ( )
C(g)+D(g)正反应速率增大的措施是 ( )
| A.增大C或D的浓度 | B.减小B或A的浓度 |
| C.减小C或D的浓度 | D.充入稀有气体 |
下列说法正确的是 ( )
| A.HF比HCl稳定是由于HF分子间存在氢键所引起的 |
| B.水在结冰时密度变小是由于水分子间存在氢键所引起的 |
| C.CH4分子很稳定,是由于分子间氢键的存在而导致的 |
| D.离子化合物肯定含有金属元素,故在微粒间不存在共价键 |