工业上用乙烯和氯气为原料合成聚氯乙烯(PVC)。已知次氯酸能跟乙烯发生加成反应:CH2=CH2+HOCl→CH2(OH)CH2Cl。以乙烯为原料制取PVC等产品的转化关系如下图所示 。
。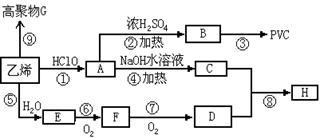
试回答下列问题:
⑴ 写出有机物B和G的结构简式:B ,G ;
⑵ ⑤、⑦的反应类型分别是 , ;
⑶ 写出D的同分异构体的结构简式 , ;
⑷ 写出反应⑥的化学方程式 ;
⑸ 写出C与D按物质的量之比为1︰2反应生成H的化学方程式
。
高铁电池是一种可逆电池,该电池能长时间保持稳定的放电电压。高铁电池总反应为3Zn+2K2FeO4+8H20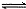 3Zn(OH)2+2Fe(OH)3+4KOH。下列判断不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列判断不正确的是
| A.放电时,负极反应为Zn-2e-+2OH一=Zn(OH)2 |
| B.充电时,阴极pH增大 |
| C.放电时,若有6mol电子转移,则正极有10 mol OH一移向负极 |
| D.充电时,阳极反应为Fe(OH)3+5OH一+3e一=FeO42-+4H2O |
水的电离常数如图两条曲线所示,曲线中的点都符合c(OH一)×c(H+)=常数,下列说法错误的是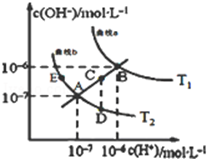
| A.图中温度T1>T2 |
| B.图中五点Kw间的关系:B>C>A=D=E |
| C.曲线a、b均代表纯水的电离情况 |
| D.若处在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液显碱性 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法不正确的是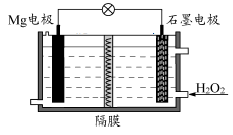
| A.Mg电极是该电池的负极 |
| B.H2O2在石墨电极上发生H2O2+2e-═2OH- |
| C.若隔膜为阳离子交换膜,则正极区有白色沉淀 |
| D.溶液中Cl-向正极移动 |
下列说法正确的是
A.温度和压强一定时,对于可逆反应:2NO2(g) N2O4(g),混合气体的密度不再改变,则反应达到平衡状态 N2O4(g),混合气体的密度不再改变,则反应达到平衡状态 |
| B.已知:H2(g)+F2(g)==="2HF(g)" ΔH=-270 kJ·mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
C.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 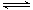 2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
| D.已知: C(s,金刚石)===C(s,石墨) ΔH=-1.5 kJ·mol-1,说明金刚石更稳定 |
将含有0.4 mol NaCl和0.5 mol Cu(NO3)2的水溶液用惰性电极电解一段时间后,在一个电极上得到0.3 mol Cu,则在另一个电极上逸出的气体(标准状况下)的体积是
| A. 4.48 L | B. 5.6L | C. 6.72L | D. 11.2L |