下列反应的离子方程式正确的是:( )
| A.向苯酚钠溶液中通入少量CO2:2C6H5O—+ CO2 +H2O → 2C6H5OH+CO32- |
B.用铜为电极电解稀硫酸溶液: 2H2O  O2↑+ 2H2 ↑ O2↑+ 2H2 ↑ |
| C.碳酸钙与醋酸反应:CO32-+2CH 3COOH = CO2↑+ H2O+2CH3COO— |
| D.Ba (OH)2溶液中加入过量Al2(SO4)3溶液: |
3Ba2++6OH-+2Al3++3SO42-="=" 3BaSO4↓+2Al(OH)3↓
氧化还原反应与四种基本类型反应的关系如右图所示,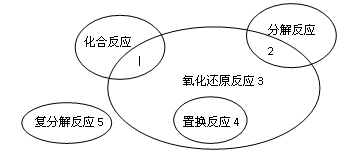
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的是()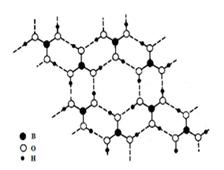
| A.正硼酸晶体属于原子晶体 |
| B.H3BO3分子的稳定性与氢键有关 |
| C.分子中硼原子最外层为8e--稳定结构 |
| D.含1molH3BO3的晶体中有3mol氢键 |
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为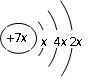 , b与c形成化合物的电子式为
, b与c形成化合物的电子式为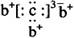 。下列比较中正确的是()
。下列比较中正确的是()
| A.原子半径:a>c>d>b | B.电负性a>b>d>c |
| C.原子序数:d>a>c>b | D.最高价含氧酸的酸性c>d>a |
对充有氖气的霓红灯管通电,灯管发出红色光。产生这一现象的主要原因()
| A.电子由激发态向基态跃迁时以光的形式释放能量 |
| B.电子由基态向激发态跃迁时吸收除红光以外的光线 |
| C.氖原子获得电子后转变成发出红光的物质 |
| D.在电流作用下,氖原子与构成灯管的物质反应 |
下图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是()
| R |
|||
| X |
|||
| Y |
|||
| Z |
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐;②Y、Z的气态氢化物水溶液的酸性Y<Z;③Z的单质常温下是液体,可与铁粉反应;④Z的原子序数比Y大19;⑤Z所在的周期中含有32种元素。
A. ①②③④ B. ①②③④⑤ C. 只有③ D. 只有①④