以下为在浓盐酸中H3AsO3与SnCl2反应的离子方程式,关于该反应的说法正确的组合是:( )
a SnCl2+b Cl-+c H3AsO3+d H+=e As+f SnCl62-+g M
①氧化剂是H3AsO3; ②M为OH-;
③每生成7.5gAs,还原剂失去的电子为0.3 mol; ④ SnCl62-是氧化产物。
| A.①③④ | B.①②④ | C.①②③④ | D.只有①③ |
下列关于同分异构体判断正确的是
| A.分子式为C2H6O的同分异构体有两个,分别是CH3OCH3和CH3CH2OH |
B.分子式为C8H10的芳香烃有3种,分别为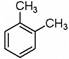 、 、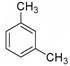 、 、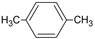 |
| C.分子式为C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3 |
D.二氯甲烷是正四面体结构, 是同一种物质 是同一种物质 |
化学工作者把烷烃、烯烃、环烷烃,转化为键数的通式,给研究有机物分子中键能大小的规律带来了很大的方便,设键数为I,则烷烃中碳原子与键数关系的通式为CnI3n+1,烯烃<视双键为两个单键>,环烷烃中碳原子与键数关系的通式均为CnI3n,则苯的同系物中碳原子与键数的关系通式为
| A.CnI3n-1 | B.CnI3n-2 | C.CnI3n-3 | D.CnI3n-4 |
1 mol有机物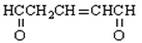 与足量的氢气和新制备的氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为
与足量的氢气和新制备的氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为
| A.1 mol 2 mol | B.1 mol 4 mol |
| C.3 mol 2 mol | D.3 mol 4 mol |
下列物质中,不能使酸性KMnO4溶液褪色的是
①乙烯 ②乙烷 ③乙苯 ④乙炔 ⑤二氧化硫 ⑥甲苯 ⑦苯 ⑧异戊二烯
| A.②③⑥ | B.②③⑤⑥⑦⑧ | C.②⑤⑦ | D.②⑦ |
将a L乙炔、b L苯、c L苯乙烯三者混合,它们所形成的混合物中碳、氢两元素的质量比是
| A.1:12 | B.1:6 | C.12:1 | D.6:1 |