有A、、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,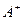 比
比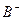 少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
(1)A单质、B单质、化合物R的熔点大小顺序为下列的 (填序号)。
①单质>B单质>R ②R>A单质>B单质
③单质>R>A单质 ④A单质>R>B单质
(2)在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体时的晶体类型为 。
(3)写出D原子的核外电子排布式 _,C的氢化物比D的氢化物在水中溶解度大得多的可能原因 。
(4)下图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体中阴、阳离子数之比为 ,FeD2物质中具有的化学键类型为 。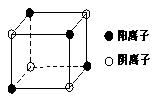
(4分) .卤代烃在氢氧化钠存在的条件下水解,这是一个典型的取代反应,其实质是带负电的原子团(例如OH-等阴离子)取代卤代烃中的卤原子。例如:
CH3CH2CH2Br+OH-(或NaOH)→CH3CH2CH2OH+Br-(或NaBr)。写出下列反应的化学方程式:
(1)溴乙烷跟NaHS反应▲。
(2)碘甲烷跟CH3COONa反应▲。
(3)由碘甲烷、无水乙醇和金属钠合成甲乙醚(CH3—O—CH2CH3) ▲、 ▲。
▲。
(6分).将Fe粉、Cu粉、FeCl3溶液、FeCl2溶液和CuCl2溶液,混合于某容器中充分反应(假定容器不参与反应),试判断下列情况下溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有▲。
(2)若氯化铜有剩余,则容器中可能有▲或▲。
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有▲,一定有▲。
(4)若氯化铁有剩余,则容器中不可能有▲。
某化学兴趣小组利用实验室提供的下列试剂:铁粉、0.1mol·L-1FeCl3溶液、0.1mol·L-1FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+的氧化性、还原性,并对实验结果加于应用。
(1)兴趣小组通过对Fe2+、Fe3+ 的价态分析,对Fe2+、Fe3+ 的氧化性、还原性提出了如下3种假设:
假设一:Fe2+具有性;
假设二:Fe2+具有性;
假设三:Fe3+具有性;
(2)设计实验方案,进行实验并描述实验现象,完成下列表格。
| 探究内容 |
实验方案 |
实验现象 |
写出下列离子方程式 |
| 探究Fe2+具有还原性 |
取少量0.1mol·L-1FeCl2溶液,加入少量KSCN溶液后,再往溶液中加入少量 |
溶液先不变红, 后变为血红色 |
①Fe2+发生的反应: |
| 探究Fe3+具有氧化性 |
取少量0.1mol·L-1FeCl3溶液,加入足量后,再往溶液中加入少量KSCN溶液 |
溶液不变为血红色 |
②Fe3+发生的反应: |
(3)该兴趣小组为说明“Fe2+具有氧化性”,提出了一个反应事实:FeCl2 + Zn ="=" ZnCl2 + Fe
该反应的离子方程式为:。
(4)根据Fe3+的性质,该兴趣小组利用FeCl3溶液腐蚀铜箔制造印刷线路板,反应的离子方程式是:。
现有失去标签的氯化钙,硝酸银,盐酸,碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编号上A.B.C.D后,产生的现象如下表所示:
| 实验内容 |
实验现象 |
|
| (1) |
A+B |
没有现象发生 |
| (2) |
B+D |
有气体放出 |
(3 ) ) |
B+C |
有沉淀生成 |
| (4) |
A+D |
有沉淀生成 |
根据实验现象按要求回答:
(1)写出A.B.C.D溶液中溶质的化学式:
A______ B_______ C_____ D______
(2)写出上述实验中有关反应的离子方程式
实验(2) B+D ___________________
实验(3) B+C __________________
某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、
盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。
其流程图如右所示(写出最佳答案)
(1).沉淀的化学式:
沉淀1,沉淀2,沉淀3;
(2).写出混合液+A的离子方程式:。
滤液+B的离子方程式:
 。
。