将铁粉放入由盐酸、MgCl2溶液、FeCl3溶液、CuCl2溶液组成的混合液中,充分反应后,铁粉有剩余,则溶液含有大量的阳离子是( )
| A.Cu2+和Fe2+ | B.H+和Cu2+ | C.Fe3+和Fe2+ | D.Fe2+和Mg2+ |
下列根据实验操作和现象所得出的结论正确的是
| 实验操作 |
实验现象 |
结论 |
|
| A |
淀粉与稀H2SO4共热,再加银 氨溶液水浴加热 |
无银镜生成 |
淀粉水解产物无还原性 |
| B |
向某溶液中先滴加氯水,再滴 加少量KSCN溶液 |
溶液变成血红色 |
溶液中含有Fe2+ |
| C |
向NaAlO2溶液中滴加饱和NaHCO3溶液 |
有白色沉淀产生 |
验证两者都发生了水解反应,且相互促进 |
| D |
将CO2通入Na2SiO3溶液中 |
有白色沉淀生成 |
证明H2CO3酸性比H2SiO3强 |
铁氧体(Fe3O4)法是处理含铬废水的常用方法,其原理是:用FeSO4把废水中Cr2O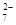 还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物(
还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物( )。处理含1 mol Cr2O
)。处理含1 mol Cr2O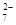 废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
| A.x=0.5,a=10 | B.x=1,a=5 | C.x=2,a=10 | D.x=0.5,a=8 |
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。有关说法不正确的是
| A.线段BC代表Fe3+ 物质的量的变化情况 |
| B.原混合溶液中n(FeBr2)=6mol |
| C.当通入Cl2 2mol时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+): n(I-): n(Br-)=2:1:3 |
下列相关反应的离子方程式书写正确的是
| A.4molFe在5molCl2中点燃反应:5Cl2+4Fe=2FeCl2+2FeCl3 |
| B.氯化铁溶液中通入硫化氢:2Fe3++H2S=2Fe2++S↓+2H+ |
| C.Ba(HCO3)2溶液中加入过量的NaOH溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
| D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀: |
Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O
下列实验现象描述正确的是
| A.碘水中加入少量裂化汽油振荡,静置后上层颜色变浅,下层颜色变为紫红色 |
| B.红热的铜丝在氯气中燃烧,产生了棕黄色的雾 |
| C.电解氯化钠饱和溶液,将阳极气体产物通入碘化钾淀粉溶液中,溶液变蓝 |
| D.溴化钠溶液中加入少量新制的氯水振荡,再加入少量四氯化碳溶液振荡,静置后上层颜色变浅,下层颜色变为橙红色 |