下列离子方程式书写正确的是
| A.向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| B.将氯气通入冷的氢氧化钠溶液中:Cl2+2OH-=Cl-+ClO-+H2O |
| C.铝片与氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑ |
| D.金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
下图是可逆反应A+2B  2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断 
A.正反应是吸热反应 B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应 D.A、B、C、D均为气体
可逆反应:2HI(g)  H2(g)+I2(g);ΔH>0。在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施
H2(g)+I2(g);ΔH>0。在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施
| A.减小容器体积 | B.降低温度 | C.加入催化剂 | D.充入H2气体 |
水的电离平衡为H2O  H+﹢OH-,△H>0,下列叙述不正确的是
H+﹢OH-,△H>0,下列叙述不正确的是
| A.将水加热,pH减小 |
| B.恒温下,向水中加入少量固体KOH,Kw不变 |
| C.向水中滴入稀醋酸,c(H+)增大 |
| D.向水中加入少量固体NaClO,平衡逆向移动 |
在0.10mol·L-1NH3·H2O溶液中,加入少量NH4Cl晶体后,引起的变化是
| A.NH3·H2O的电离程度减小 |
| B.NH3·H2O的电离常数增大 |
| C.溶液的导电能力不变 |
| D.溶液的pH增大 |
下列关于左图装置的说法正确的是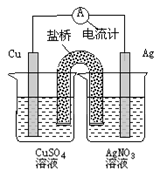
| A.银电极是负极 |
| B.铜电极上发生的反应为Cu-2e-=Cu2+ |
| C.外电路中的电子是从银电极流向铜电极。 |
| D.该装置能将电能转化为化学能 |