下列化学用语书写正确的是
| A.乙醇的结构简式:C2H5OH | B.氯化钠的电子式: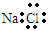 |
C.S2-离子的结构示意图: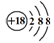 |
D.有8个质子、10个中子的核素:168O |
下列各种溶液粒子物质的量浓度关系正确的是()
A.0.1mol·V的NH4Cl溶液与0.05mol·L-1的NaOH溶液等体积混合:c(Cl-)>c(Na+)>c(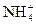 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
B.0.2mol·L-1Na2CO3溶液:c(OH-)=c(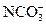 )+c(H+)+2c(H2CO3) )+c(H+)+2c(H2CO3) |
C.0.2mol·L-1(NH4)2SO4溶液:c(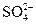 )>c( )>c(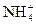 )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
D.0.2mol·L-1NaHCO3溶液:c(Na+)>c(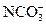 )>c( )>c(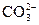 )>c(OH-) )>c(OH-) |
25℃时,pH=7的(NH4)2SO4与NH3·H2O的混合液中,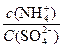 的值是()
的值是()
| A.2∶1 | B.大于2∶1 |
| C.小于 2∶1 | D.无法判断 |
在25℃时,pH等于11的NaOH溶液和NaCN溶液,两溶液中水的电离度大小的比较正确的是()
| A.相等 | B.后者比前者大11倍 |
| C.后者是前者的108倍 | D.前者是后者的108倍 |
下列物质在常温下发生水解时,对应的离子方程式正确的是()
A.Na2CO3: +2H2O +2H2O H2O+CO2↑+2OH- H2O+CO2↑+2OH- |
B.NH4NO3: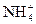 +H2O +H2O NH3·H2O+H+ NH3·H2O+H+ |
C.CuSO4:Cu2++H2O Cu(OH)2+2H+ Cu(OH)2+2H+ |
| D.KF:F-+H2O====HF+OH- |
下列离子分别加入纯水中,能使水中c(OH-)增大的是()
| A.Cl- | B.ClO- | C. |
D.Na+ |