(1)写出实验室制NH3的反应方程式为 ;
(2)硝酸具有强氧化性,它能和许多物质发生反应。写出浓硝酸与非金属单质碳的反应方程式。 。
配平下列化学(或离子)方程式:
(3)__FeCl2 + __KNO3 + __HCl — __FeCl3 + __KCl + __NO↑ + __H2O
(4)__SO3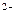 +__MnO4
+__MnO4 +__H
+__H —__Mn
—__Mn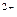 +__SO4
+__SO4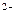 +__H2O
+__H2O
现有电解质溶液:①Na2CO3②NaHCO3
③NaAlO2④CH3COONa⑤NaOH。
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是__________(填编号)。
(2)将上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,pH变化最大的是__________(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,无气体产生的是__________(填编号)。
(4)将上述①②③④四种电解质溶液混合,发生反应的离子方程式为__________。
我国能源以煤为主,燃煤产生的二氧化硫的年排放量为1825吨,居世界首位。二氧化硫在湿度较大的大气中,在烟尘中的金属离子作用下会发生催化氧化反应,形成酸雾,其化学方程式是__________________________________________________________。
随着我国人民生活水平的不断提高,家用热水器走入寻常百姓家。目前家用热水器主要有电热水器和燃气热水器两种。燃气热水器又可分为天然气型、人工煤气型和液化石油气型等。
(1)某城市人工煤气是由水煤气和焦炉煤气混合而成的。写出由焦炭制取水煤气的化学方程式____________________________________________________________________________。
(2)将40 L 20 ℃冷水加热到80℃。若使用天然气热水器,则需要标准状况下____________L 甲烷(已知22.4 L甲烷燃烧放出890.4 kJ热量,假设甲烷燃烧时的热效率为60%,水的比热为4.18 kJ·kg-1·℃-1)。若使用电热水器,则需要通电___________分钟(假设电加热棒功率为1 500 W,热效率为80%)。
(3)煤气和电都是二次能源,制煤气和火力发电都要消耗能源,且产生大气污染物,未来的新型能源是_____________________________。
同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成还是分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(s,白磷)+5O2(g)====P4O10(s)
ΔH="-2" 983.2 kJ·mol-1①
P(s,红磷)+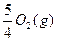 ====
====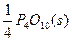
ΔH="-738.5" kJ·mol-1②
则白磷转化为红磷的热化学方程式为_________。相同状况下,能量状态较低的是_________;白磷的稳定性比红磷_________(填“高”或“低”)。
如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5 mL稀盐酸,试完成下列问题。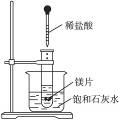
(1)实验中观察到的现象是__________________。
(2)产生上述现象的原因是__________________。
(3)写出有关反应的离子方程式__________________。
(4)由实验推知,MgCl2溶液和H2的总能量__________________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。