对实验Ⅰ~Ⅳ的实验现象预测正确的是
| A.实验Ⅰ:液体分层,下层呈无色 |
| B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C.实验Ⅲ:试管中溶液颜色变为红色 |
| D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
室温下,若溶液中由水电离产生的c(OH-)=1×10-14mol/L,满足此条 件的溶液中一定可以大量共存的离子组是()
件的溶液中一定可以大量共存的离子组是()
| A.Al3+、Na+、NO3-、Cl- | B.K+、Na+、Cl-、NO3- |
| C.K+、Na+、Cl-、AlO2- | D.K+、NH4+、SO42-、NO3- |
可以判定某酸(HA)是强电解质的事实是()
A.该酸加热至沸腾不分解 B.该酸与CaCO3反应放出CO2
C.该酸可以溶解Cu(OH)2D.0.01 mol/L该酸的pH=2
升高温度,下列数据不一定同时增大的是()
| A.化学反应速率v | B.弱电解质的电离平衡常数Ka |
| C.化学平衡常数K | D.水的离子积常数KW |
如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)()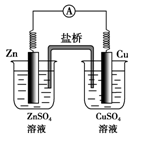
| A.反应中,盐桥中的K+会移向CuSO4溶液 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.铜片上有气泡逸出 |
| D.反应前后铜片质量不改变 |
关于原电池的叙述正确的是()
A.构成原电池的正极和负极必须是 两种不同金属 两种不同金属 |
| B.在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l) ΔH<0,设计成原电池 |
| C.在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D.原电池工作时,正极和负极上发生的都是氧化还原反应 |