某温度下, 的平衡常数
的平衡常数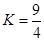 .该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是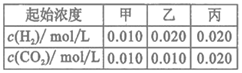
| A.平衡时,乙中CO2的转化率大于60% |
| B.平衡时,甲中和丙中H2的转化率均是60% |
| C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L |
| D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
下图是一套检验气体性质的实验装置,向装置中缓缓地通入X气体,若关闭活塞K,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色。据此判断X气体和洗气瓶内液体Y可能是()
| A |
B |
C |
D |
|
| X |
CO |
SO2 |
CO2 |
Cl2 |
| Y |
浓H2SO4 |
饱和NaHCO3溶液 |
Na2SO3溶液 |
饱和NaCl溶液 |
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性强弱的顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是( )
A.2Fe3++SO2+2H2O====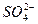 +4H++2Fe2+ +4H++2Fe2+ |
B.I2+SO2+2H2O====H2SO4+2HI |
C.H2O2+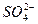 +2H+====SO2↑+O2↑+2H2O +2H+====SO2↑+O2↑+2H2O |
D.2Fe3++2I-====2Fe2++I2 |
向100 mL含等物质的量的HBr和H2SO3的溶液里通入0.01 mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。则原溶液中HBr的物质的量浓度为( )
| A.0.007 5 mol·L-1 | B.0.008 mol·L-1 |
| C.0.075 mol·L-1 | D.0.08 mol·L-1 |
下列变化的实质相似的是()
| A.SO2和Cl2均可使品红试液褪色 |
| B.浓H2SO4和稀H2SO4与金属反应时都放出气体 |
| C.HBr和HI不能用浓H2SO4与NaBr、NaI反应制取 |
| D.浓H2SO4和浓盐酸在空气中敞口存放浓度都会下降 |
储存浓H2SO4的铁罐外口常会出现严重的腐蚀现象,这体现了()
| A.浓H2SO4的吸水性和酸性 | B.浓H2SO4的脱水性和吸水性 |
| C.浓H2SO4的强氧化性和吸水性 | D.浓H2SO4的吸水性和稀H2SO4的通性(酸性) |