用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1 molCu(OH)2后恰好恢复到电解前的浓度和pH。则电解过程中转移的电子数为:( )
| A.0.1mol | B.0.2mol | C.0.3mol | D.0.4mol |
常温下,用Na2SO3溶液吸收SO2时,溶液pH随n(SO32-):n(HSO3-)变化的关系如下表:
| n(SO32-):n(HSO3-) |
91:1 |
1:1 |
9:91 |
| pH |
8.2 |
7.2 |
6.2 |
以下离子浓度关系的判断正确的是
A.NaHSO3溶液中c(H+)<c(OH-)
B.Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+)
D.当吸收液呈中性时,c(Na+)= c(HSO3-)+2 c(SO32-)
用气体传感器可以检测汽车尾气中CO的含量。传感器是以燃料电池为工作原理,其装置如右图所示,该电池中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是
A.负极的电极反应式为:CO+O2-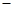 2e-=CO2 2e-=CO2 |
| B.工作时电子由电极a通过传感器流向电极b |
| C.工作时电极b作正极,O2-由电极a流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
下列叙述正确的是
| A.加入铝粉能产生H2的溶液中可能大量共存的离子组:NH4+、Fe2+、SO42-、NO3- |
| B.常温下由水电离出的H+与OH-的浓度积为10-20mol2·L-2的溶液中可能大量共存的离子组:Na+、S2-、Cl-、CO32- |
| C.向FeI2溶液中通入过量Cl2的离子方程式:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.向Ca(ClO)2溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+CO32- |
下列对检验方法或现象描述不正确的是
| A.乙烷中是否混有乙烯,可用通过溴水是否退色进行检验 |
| B.乙醇中是否混有水,可用加硫酸铜粉末是否变蓝进行检验 |
| C.乙酸中是否混有乙酸,可用加入金属钠是否产生气体进行检验 |
| D.乙酸乙酯是否混有乙酸,可用加石蕊试液是否变红进行检测 |
短周期元素X、Y、Z、W、Q在周期表中的位置如图所示。下列说法不正确的是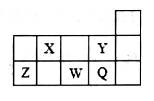
| A.元素的非金属性Y>Q,但其同浓度氢化物水溶液的酸性,HY<HQ |
| B.形成简单离子的半径从小到大的顺序是Y<Q<W |
| C.Z的最高价氧化物可溶于水,也能溶于强碱溶液 |
| D.X的气态氢化物浓溶液可用于检验管道氯气的泄漏 |