常温下,下列各溶液中能大量共存的离子组是( )
| A.由水电离出的c(H+) = 10-12 mol·L-1 的溶液中:Na+、Ca2+、K+、HSO3- |
| B.在pH = 2的的溶液中:Fe2+、I-、NO3-、Cl- |
| C.c(OH-) = 10-12 mol·L-1 的溶液中: K+、SO42-、Cl-、HCO3- |
| D.使酚酞试液呈红色的溶液中:Na+、AlO2-、NO3-、SO42- |
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。某校课外兴趣小组以两条途径分别对X进行如下实验探究:
途径a: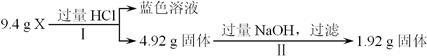
途径b:
下列有关说法不正确的是( )
| A.1.92 g固体只含Cu |
| B.由Ⅰ可知X中一定存在Fe2O3和Cu |
| C.原混合物中m(Fe2O3)∶m(Cu)=1∶1 |
| D.原混合物X至少含Al2O3和SiO2中的一种,但不能进一步确认二者的存在与否 |
在一定条件下,将0.1 L CO、0.2 L CO2、0.1 L NO、0.2 L NO2和0.2 L NH3混合,然后通过分别盛有足量蒸馏水、饱和碳酸氢钠溶液和氢氧化钠溶液的三个洗气瓶(洗气瓶排列顺序不确定)。假设气体通过每个洗气瓶都能充分反映,则尾气(已干燥) ( )
| A.不可能是单一气体 | B.不可能含有一氧化碳 |
| C.可能存在原气体中的两种气体 | D.成分与洗气瓶的排列顺序无关 |
下列与有机物结构、性质相关的叙述错误的是 ( )
A.乙醛和丙烯醛( )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B.一分子β-月桂烯( )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C.用甘氨酸( )和丙氨酸( )和丙氨酸( )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D. 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
下列说法不正确的是 ( )
| A.均三甲苯在核磁共振氢谱中能出现两组峰,且其峰面积之比为3∶1 |
B.按系统命名法,化合物 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 |
C.结构片段为 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 |
D.肌醇 与葡萄糖 与葡萄糖 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 |
下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是 ( )
| 选项 |
离子组 |
加入试剂 |
加入试剂后发生反应的离子方程式 |
| A |
NH 、Fe2+、SO 、Fe2+、SO |
少量Ba(OH)2溶液 |
2NH +SO +SO +Ba2++2OH-===BaSO4↓+2NH3·H2O +Ba2++2OH-===BaSO4↓+2NH3·H2O |
| B |
Mg2+、HCO 、Cl- 、Cl- |
过量NaOH溶液 |
Mg2++2HCO +4OH-===2H2O+Mg(OH)2↓+2CO +4OH-===2H2O+Mg(OH)2↓+2CO |
| C |
K+、NH3·H2O、CO |
通入少量CO2 |
2OH-+CO2===CO +H2O +H2O |
| D |
Fe2+、NO 、HSO 、HSO |
NaHSO4溶液 |
HSO +H+===SO2↑+H2O +H+===SO2↑+H2O |