零排放燃料电池曾被美国《时代》杂志列为21世纪改变人类生活的十大新科技之首。其中最具代表意义的质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极。下列说法中不正确的是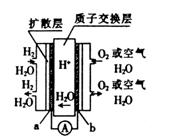
| A.a极为该电池的负极 |
| B.该电池的正极反应式为O2 + 4H+ + 4e- =2H2O |
| C.该电池的能量转化主要形式是化学能转化为电能 |
| D.H+(质子)由正极移动至负极 |
下列装置或操作不能达到目的的是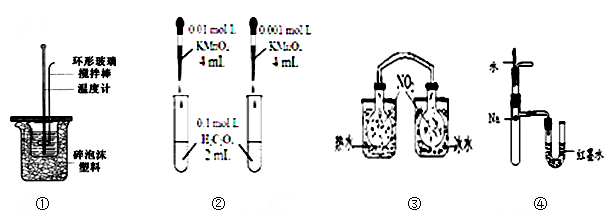
| A.装置①用于滴定中和热装置 |
| B.装置②依据褪色快慢比较浓度对反应速率的影响 |
C.③依据两容器内气体颜色变化,判断反应2NO2(g)  N2()O4(g)平衡移动的方向 N2()O4(g)平衡移动的方向 |
| D.装置④依据U管两边液面的高低判断Na和水反应的热效应 |
一定温度下将0.2 mol气体A充入10 L恒容密闭容器中,进行反应:
2A(g)+B(g) 2C(g)+D(s) △H<0,一段时间后达到平衡,此反应过程中测定的数据如下表所示,则下列说法正确的是
2C(g)+D(s) △H<0,一段时间后达到平衡,此反应过程中测定的数据如下表所示,则下列说法正确的是
| t/min |
2 |
4 |
6 |
8 |
10 |
| n(A)/mol |
0.16 |
0.13 |
0.11 |
0.10 |
0.10 |
A.反应前2 min的平均速率ν(C) ="0.02" mol·L-1·min-1
B.平衡后降低温度,反应达到新平衡前ν(逆)> ν(正)
C.其他条件不变,10 min后再充入一定量的A,平衡正向移动,A的转化率变小
D.保持其他条件不变,反应在恒压下进行,平衡时A的体积分数与恒容条件下反应相同
在容积固定的密闭容器中,进行下列反应A(g)+B(g) 2C(?)+D(g),此反应符合下列两个图像(其中φ代表物质的百分含量),则下列判断正确的是( )
2C(?)+D(g),此反应符合下列两个图像(其中φ代表物质的百分含量),则下列判断正确的是( )
| A.物质C不可能为气态 |
| B.正反应为吸热反应 |
| C.该反应,升高温度平衡正向移动 |
| D.300℃下该反应到达平衡状态后,迅速充入He,平衡正向移动 |
工业上制备纯硅的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g) ΔH=+Q KJ·mol-1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是( )
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则在平衡时,吸收热量为Q kJ |
| C.将反应的温度由T1升高至T2,则对应温度下的平衡常数K1> K2 |
| D.当反应吸收热量为0.25 Q kJ时,生成的HCl恰好与1 mol NaOH反应 |
25℃、101kPa下,4g CH4完全燃烧生成CO2和液态水时,放出222.5 kJ的热量,则下列热化学方程式中正确的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2 H2O(g ) △H=-890kJ/mol |
| B.CH4(g)+2O2(g)=CO2(g)+2 H2O(l ) △H=+890kJ/mol |
C. CH4(g)+O2(g)= CH4(g)+O2(g)=  CO2(g)+H2O(1) △H=-445kJ/mol CO2(g)+H2O(1) △H=-445kJ/mol |
| D.CH4(g)+2O2(g)=CO2(g)+2 H2O(l ) △H=-890kJ |