镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是
A.充电时阳极反应:Ni(O H)2-e- + OH- ="=" NiOOH + H2O H)2-e- + OH- ="=" NiOOH + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
【改编】下列说法中,不正确的是
| A.反应热指的是反应过程中放出或吸收的热量 |
| B.原电池的正极发生氧化反应 |
| C.化学变化一定伴随能量变化 |
| D.升温反应速率一定加快 |
【改编】下列离子方程式正确的是
| A.将铁和铜用导线连接后同时插入硝酸银溶液中,铜上的电极反应为:Cu-2e-=Cu2+ |
| B.FeBr2溶液中通入少量的Cl2:Cl2+2Fe2+= 2Fe3++2Cl- |
| C.将金属钠放入硫酸铜溶液中:2Na+Cu2+-=2Na++Cu |
| D.酸性氢氧燃料电池的正极反应:H2-2e-= 2H+ |
下列有关能量转化的说法中正确的是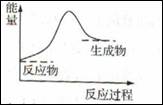
| A.铝热反应属于吸热反应 |
| B.“H—Cl→H+C1"过程中放出热量 |
| C.干冰升华过程放出热量 |
D.反应“C+H2O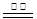 CO+H2”中的能量变化可以用上图表示 CO+H2”中的能量变化可以用上图表示 |
将0.1 mol N2和0.3 mol H2置于密闭容器中发生反应:N2+3H2 2NH3,下列关于该反应的说法中正确的是
2NH3,下列关于该反应的说法中正确的是
| A.增大压强,反应速率减小 |
| B.最终可生成0.2 mol NH3 |
| C.升髙温度,反应速率增大 |
| D.当V正(N2):V 正(H2)=1:3时,一定达化学平衡状态 |
将铁片和碳棒按下图所示方式插入硫酸铜溶液中,电流计指针发生偏转。下列针对该装罝的说法,正确的是
| A.碳棒是正极 |
| B.该装置能将电能转化为化学能 |
| C.外电路中电流由铁片流出经过电流计流向碳棒 |
| D.该装置的总反应为:2Fe+3Cu2+=2Fe3++3Cu |