有A、B、C、D、W五种元素。W的原子序数为29,其余的均为短周期主族元素;其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个未成对的电子;C元素氢化物与其最高价氧化物对应水化物之间反应生成一种盐;D原子核内的质子 数与中子数相等,能与B形成DB2、DB3常见化合物。根据以上条件,回答下列问题:
数与中子数相等,能与B形成DB2、DB3常见化合物。根据以上条件,回答下列问题:
(1)推断元素名称:A 。
(2)C元素的氢化物的空间构型为 ,分子中的化学键 (填“有”或“无”)极性,其分子为 分子(填“极性”或“非极性”)。
(3)比较A、B、C三种元素的第一电离能由大到小的顺序 (用元素符号表示),A、B、C三种元素的氢化物的沸点高低 (用化学式表示)。
(4)写出D元素原子基态时的电子排布式 ,其在元素周期表中的位置 。
(5)W元素+2价离子的水溶液呈现天蓝色,是该离子与水分子通过 键形成的 (填化学式)而显示出的颜色。
食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
| 品名 |
蔬菜苏打饼 |
| 配料 |
面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁、食品添加剂(碳酸氢钠) |
| 保质期 |
十二个月 |
| 生产日期 |
2010年11月6日 |
(1)对上表中各种配料成分的理解,不正确的是()。
A.富含蛋白质的是鲜鸡蛋
B.富含维生素的是脱水青菜和橙汁
C.富含淀粉的是面粉和白砂糖
D.富含油脂的是精炼食用植物油和奶油
(2)以今天的日期为准,该饼干能否食用( 填“是”或“否”)原因是
(3)上表中碳酸氢钠是作为,其原理是(用化学方程式表示)
糖类物质提供了人体需要的75%的热量,因此葡萄糖对人体的健康尤为重要,试根据你已有知识,回答下列问题:
(1)糖尿病一直折磨着很多病人的身心健康,某同学根据自己所学知识,设计实验用某病人的尿液作了实验,发现做实验的试管内壁上产生了闪亮的银,从而得出结论,该病人尿液中含葡萄糖,该病人患有糖尿病,现欲将试管内壁银镜清洗干净,最好使用下列的()
A.乙醛溶液 B.浓硝酸溶液 C.稀盐酸溶液 D.稀硝酸溶液
(2)能说明葡萄糖是一种单糖的主要理由是()
A.糖类物质中含碳原子数最少 B.不能再水解成更简单的糖
C.分子中只有一个醛基 D.糖类中结构最简单的物质
(3)我们将连有4个不同基团的碳原子称为手性碳原子,含手性碳原子的物质通常具有不同的光学特征(称为光学活性), 具有一定的光学活性,请你列举两种使该物质失去光学活性的方法____________________________________。
具有一定的光学活性,请你列举两种使该物质失去光学活性的方法____________________________________。
脂肪、淀粉、蛋白质被称为人类的三大营养物质,它们的共同性质是都与水发生________反应。我们从食物中摄取的蛋白质,在胃液中的胃蛋白酶和胰蛋白酶的作用下________反应,生成________,它被人体吸收后,重新合成人体所需要的各种________,人体内各组织的蛋白质不断分解,最后主要生成________排出体外。
某天然油脂A的分子式为C57H106O6。1 mol该油脂水解可得到1 mol甘油、1 mol不饱和脂肪酸B和2 mol直链饱和脂肪酸C。经测定B的相对分子质量为280,原子个数比为C∶H∶O=9∶16∶1。
(1)写出B的分子式:__________________。
(2)写出C的结构简式:__________________;C的名称是____________________。
(3)写出含5个碳原子的C的同系物的同分异构体的结构简式:
________________________________________________________________________
________________________________________________________________________。
如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应。A.B.C都可以被强还原剂还原成为D(C6H14O6)。B脱水可得到五元环的酯类化合物E或六元环的酯类化合物F。
已知,相关物质被氧化的难易次序是:RCHO最易,R—CH2OH次之,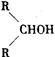 最难。请在下列空格中填写A.B.C.D.E、F的结构简式。
最难。请在下列空格中填写A.B.C.D.E、F的结构简式。
A:B:C:
D:E:F: