铝粉与某些金属氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应。
如:2Al+Fe2O3 2Fe+Al2O3,反应发生时放出大量的热。仔细阅读上述信息回答下列问题:
2Fe+Al2O3,反应发生时放出大量的热。仔细阅读上述信息回答下列问题:
(1)“铝热反应”属于四种基本反应类型中的_________________反应。
(2)信息中的“某些”指________(填“比铝活泼的”“比铝不活泼的”或“任意”)。
(3)试写出铝粉与MnO2发生的铝热反应方程式
_______________________________________________________。
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g)+O2(g)  2NO(g) ΔH,已知该反应在 T ℃时,平衡常数K=9.0。
2NO(g) ΔH,已知该反应在 T ℃时,平衡常数K=9.0。
请回答:
(1)已知:N2(g)+2O2(g)  2NO2(g)ΔH12NO2(g)
2NO2(g)ΔH12NO2(g)  O2+2NO(g)ΔH2 ΔH=(用含ΔH1、ΔH2的表达式表示);
O2+2NO(g)ΔH2 ΔH=(用含ΔH1、ΔH2的表达式表示);
(2)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.5 mol,则NO的反应速率;
(3)假定该反应是在恒容条件下进行,下列能判断该反应已达到平衡的是________;
| A.消耗1 mol N2同时生成1 mol O2 |
| B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 |
| D.2v正(N2)=v逆(NO) |
(4)下图是反应N2(g)+O2(g)  2NO(g)的“K-T”、“c(NO)-t”图,由图A可以推知该反应为反应(填“吸热”或“放热”)。由图B可知,与a对应的条件相比,b改变的条件可以是;
2NO(g)的“K-T”、“c(NO)-t”图,由图A可以推知该反应为反应(填“吸热”或“放热”)。由图B可知,与a对应的条件相比,b改变的条件可以是;
(5)T ℃时,某时刻测得容器内N2、O2、NO的浓度分别为0.20 mol·L-1、0.20mol·L-1和0.50mol·L-1,此时反应N2(g)+O2(g)  2NO(g)________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),平衡时,N2在混合气体的体积百分数为多少?(在答题卡上写出具体计算过程,结果保留2位有效数字)
2NO(g)________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),平衡时,N2在混合气体的体积百分数为多少?(在答题卡上写出具体计算过程,结果保留2位有效数字)
化合物A最早发现于酸奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得。工业上也可由丙烯经过下列方法合成:
回答下列问题:
(1)写出下列反应的反应方程式,并注明反应类型: :反应类型:
:反应类型: :反应类型:;
:反应类型:;
(2)A的结构简式为:, 浓硫酸加热条件下两分子的A能反应生成六元环状化合物,写出该化合物的结构简式:;
(3)D的含氧官能团名称为:(写出一种即可),已知D的一种同分异构体能和NaHCO3溶液反应放出气体,写出该同分异构体的结构简式:;
(4) 在一定条件下容易发生“脱羧”反应,产物之一为甲醛的同系物,写出该产物的结构简式:。
在一定条件下容易发生“脱羧”反应,产物之一为甲醛的同系物,写出该产物的结构简式:。
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:
已知:反应Ⅱ包含2NaHSO3 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式:。
(2)“灼烧”时发生反应的化学方程式:。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:。
(4)副产品X的化学式是:;可循环利用的物质是:_____________。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约
为。
(6)检验产品中含有碳酸钠杂质所需试剂是(填编号)
①酸性高锰酸钾②品红溶液③澄清石灰水④饱和碳酸氢钠溶液⑤NaOH⑥稀硫酸
CO2和CO是工业排放的对环境产生影响的废气。
(1)以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);ΔH=a kJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol-1
则a为。
(2)科学家们提出用工业废气中的CO2制取甲醇:CO2+3H2CH3OH+H2O。制得的CH3OH可用作燃料电池的燃料。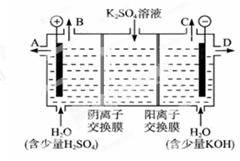
①在KOH介质中,负极的电极反应式为_________________________________。
②作介质的KOH可以用电解K2SO4溶液的方法制得。则KOH在_______出口得到,阳极的电极反应式是:_____________________________________。
(3)利用CO与H2反应可合成CH3OCH3。
已知:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2(g),ΔH=-247kJ/mol
CH3OCH3(g) + CO2(g),ΔH=-247kJ/mol
在一定条件下的密闭容器中,该反应达到平衡,要提高CO的转化率,可以采取的措施是.
| A.低温高压; | B.加入催化剂; | C.体积不变充入氦气; | D.增加CO的浓度;E.分离出二甲醚 |
(4)CH3OCH3也可由CH3OH合成。已知反应2CH3OH(g)  CH3OCH3(g) + H2O(g),在某温度下,在1L密闭容器中加入CH3OH ,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
CH3OCH3(g) + H2O(g),在某温度下,在1L密闭容器中加入CH3OH ,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.01 |
0.2 |
0.2 |
①0-10 min内反应速率v(CH3OH) = 。
②该温度下的平衡常数为。
③若平衡后,再向容器中再加入0.01mol CH3OH和0.2mol CH3OCH3,此时正、逆反应速率的大小:
v正v逆 (填“>”、“<”或“=”)。
莫沙朵林是一种镇痛药,它的合成路线如下:
(1)化合物D中含氧官能团的名称为。
(2)下列说法正确的是_________
| A.1 mol B可以与4 mol CH3COOH发生酯化反应 |
| B.C的分子式为C5H4O2 |
| C.D→E的反应是加成反应 |
| D.E可以发生消去反应,F可与HCl反应 |
(3)C与新制氢氧化铜反应的化学方程式为。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式:。
I.核磁共振氢谱有4个峰; Ⅱ.能发生银镜反应和水解反应; Ⅲ.能与FeCl3溶液发生显色反应。
(5)已知E+X→F为加成反应,化合物X的结构简式为。
(6)已知: 。化合物
。化合物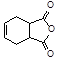 是合成抗病毒药阿昔洛韦的中间体,它可以用
是合成抗病毒药阿昔洛韦的中间体,它可以用 经氧化、消去、成酐一系列反应后再和原料M合成。
经氧化、消去、成酐一系列反应后再和原料M合成。
①则M的结构简式为
②其中的消去反应的化学方程为: