双氧水(过氧化氯)被称作“最清洁”的化学品,在纺织业和造纸业主要用作漂白剂,在化工合成中用作氧化剂和环氧化剂,在食品和医药工业中用作消毒剂、杀菌剂。目前,世界上过氧化氢的生产方法主要有电解法、葸醌法等。
I、电解法中成本最低的是过硫酸铵法
电解所用电槽以铂为阳极,以铅或石墨为阴极;NH4HSO4水溶液经阴极室,再作为阳极液从阳极室流出,得(NH4)2S2O8溶液,电解总反应式: 溶液送往水解器中减压水解、蒸发,蒸出过氧化氢的水溶液,剩余溶液流到阴极室再循环使用。
溶液送往水解器中减压水解、蒸发,蒸出过氧化氢的水溶液,剩余溶液流到阴极室再循环使用。
(1)写出过氧化氢的电子式 。
(2)写出水解器中(NH4)2S2O8溶液的水解方程式 。
(3)铂价格昂贵,试分析电槽阳极用铂不用铅的原因 。
(4)试分析水解器中使用减压水解、蒸发的原因 。
Ⅱ、葸醌法是国内外大规模生产过氧化氢普遍采用的方法,生产简易流程图如下所示:
其中,触媒为催化剂,工作液为乙基葸醌与有机溶剂的混合液,主要反应方程式为:
(1)写出流程图中加“?”的操作 。
(2)写出流程图中再生使用物质的名称 。
(3)根据双氧水生产的特点,工业液中有机溶剂的选择很重要。理想的有机溶剂应满足以下要求:①对乙基葸醌和氢乙基葸醌具有良好的溶解能力:②粘度低,沸点高,难挥发,着火点高;③低毒性。请分析再写出两点要求:④ ;⑤ 。
某同学进行试验探究时,欲配制1.0molL-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。
为探究原因,该同学查得Ba(OH)2·8H2O 部分溶解度数据,见下表:
| 温度 |
283K |
293K |
303K |
| 溶解度(g/100g H2O) |
2.5 |
3.9 |
5.6 |
(1)烧杯中未溶物仅为BaCO3,理由是。
(2)假设试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题纸上写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 |
预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 |
###### |
| 步骤2:取适量滤液于试管中,滴加稀硫酸。 |
_______________________ |
| 步骤3:取适量步骤1中的沉淀于试管中, ,连接带塞导气管将产生的气体导入澄清石灰水中。 |
_______________________ ______________________ |
| 步骤4:取步骤1中的滤液于烧杯中,______________________________ |
_______________________,说明该试剂中含有Ba(OH)2。 |
(3)将试剂初步提纯后,准确测定其中Ba(OH)2·8H2O的含量。
实验如下:①配制250 mL 约0.1mol·L-1Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,搅拌,将溶液转入,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将(填“0.020”、“0.05”、“0.1980”或“1.5”)molL-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
(4)室温下,(填“能”或“不能”) 配制1.0 mol·L-1Ba(OH)2溶液,说明理由________________________________________________________________________________________.
二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是氯气与硫合成二氯化硫的实验装置。
试回答下列问题:
(1)装置A中发生反应的化学方程式为。
(2)装置B、C应盛放的药品分别是、。
(3)实验开始前先在D中放一定量的硫粉.加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是。
(4)实验时,D装置需加热至50—59℃.最好采用的措施是、如何防止E中液体挥发?。
(5)F装置中干燥管内所盛物质是,作用是。
(6)由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为。
甲.乙两个研究性学习小组为测定氨分子中氮.氢原子个数比,设计了如下实验流程:
下图A.B.C为甲.乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
实验开始前装置中的空气已排尽。甲小组测得:反应前氧化铜的质量为 .氧化铜反应后剩余固体的质量为
.氧化铜反应后剩余固体的质量为 .生成氮气在标准状况下的体积
.生成氮气在标准状况下的体积 。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。
。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。
(1)写出仪器a的名称:。
(2)甲.乙两小组选择了不同方法制取氨气,请将实验装置的字母编号和制备原理填写在下表空格中。
| 实验装置 |
实验药品 |
制备原理 |
|
| 甲小组 |
A |
氢氧化钙.硫酸铵 |
反应的化学方程式为 ① |
| 乙小组 |
② |
浓氨水.氢氧化钠 |
用化学平衡原理分析氢氧化钠的作用: ③ |
(3)甲小组用所测数据计算出氨分子中氮.氢的原子个数之比为。
(4)在操作和计算正确的情况下,乙小组用所测数据计算出氨分子中氮.氢的原子个数比明显小于理论值,其原因可能是。
(5)乙小组在原有实验的基础上增加了一个装有药品的实验仪器,重新实验,得出合理的实验结果。该药品的名称是。
银镜反应是检验醛基的重要反应,教材对该实验的操作条件只是粗略的描述。某同学进行如下研究:
(1)在干净试管中加入2ml2%,然后,得到银氨溶液,分装入5支试管,编号为1#.2#.3#.4#.5# 。
(2)依次滴加2%.5%.10%.20%.40%的乙醛溶液4滴,快速振荡后置于60℃~70℃的水浴中。3分钟后,试管1#未形成大面积银镜,试管5# 的银镜质量差有黑斑, 试管4# 产生的银镜质量一般,试管2#.3# 形成光亮的银镜。
该研究的目的是:。
(3)乙醛发生银镜反应的化学方程式为:,
(4)有文献记载:在强碱性条件下,加热银氨溶液可能析出银镜。验证和对比实验如下。
| 装置 |
实验序号 |
试管中的药品 |
现象 |
 |
实验Ⅰ |
2mL银氨溶液和数滴较浓NaOH溶液 |
有气泡产生: 一段时间后,溶液逐渐变黑:试管壁附着银镜 |
| 实验Ⅱ |
2mL银氨溶液和 数滴浓氨水 |
有气泡产生:一段时间后,溶液无明显变化 |
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料后,得知:
a.Ag(NH3)2++2H2O Ag++2NH3·H2O b.AgOH不稳定,极易分解为黑色Ag2O
Ag++2NH3·H2O b.AgOH不稳定,极易分解为黑色Ag2O
经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O。产生Ag2O的原因是:
。
(5)用湿润的红色石蕊试纸检验NH3产生的现象是 。用稀HNO3清洗试管壁上的Ag,该反应的化学方程式是 。
(6)该同学对产生银镜的原因提出假设:在NaOH存在下,可能是NH3还原Ag2O。如果该假设成立,则说明检验醛基时,银氨溶液不能呈强碱性,因为:
某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去)。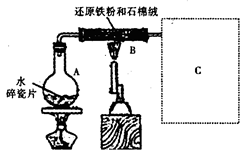
(1)装置B中发生反应的化学方程式是。
(2)虚线框图C的气体收集装置是下图中的(选填字母编号)。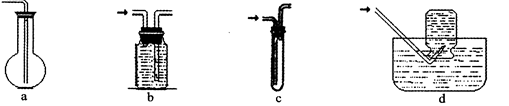
(3)反应停止,待B管冷却后,称量,得到固体质量为28.8g。再向固体中加入过量稀盐酸充分反应,并进行如下实验: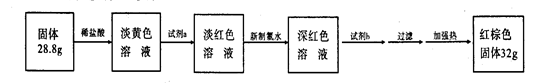
试剂a的化学式是,试剂b的化学式是;加入新制氯水后溶液红色加深的原因是(用离子方程式表示)。
(4)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现请对褪色原因进行探究。首先提出假设。假设1:溶液中的+3价铁被氧化为更高的价态;假设2:
;为了对所提出的假设2进行验证,实验方案是
。
(5)根据所给数据,可计算出反应后B装置中铁元素的质量分数为。