设nA为阿伏加德罗常数的数值,下列说法错误的是
| A.1molNH3中含有3nA个N-H键 |
| B.0.1mol/L Na2CO3溶液中含有0.1nA个CO32- |
| C.标准状况下,11.2L CO2中含有nA个O原子 |
D.20g重水( )中含有10nA个个电子 )中含有10nA个个电子 |
某有机物其结构简式为下图,关于该有机物下列叙述正确的是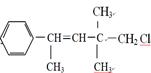
| A.不能使酸性KMnO4溶液褪色 |
| B.不能发生取代反应 |
| C.在加热和催化剂作用下,最多能和4 mol H2反应 |
| D.一定条件下,能和NaOH醇溶液反应 |
2011年,在欧洲一些国家发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质二恶英,其结构为 ,已知它的二氯代物有10种,则其六氯代物有
,已知它的二氯代物有10种,则其六氯代物有
| A.5种 | B.11种 | C.10种 | D.5种 |
分子式为C7H8O的芳香化合物中,与FeCl3溶液混合显紫色和不显紫色的物质分别有
| A.2种和1种 | B.2种和3种 |
| C.3种和2种 | D.3种和1种 |
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:
①蒸馏 ②过滤 ③静置分液 ④加入足量的金属钠 ⑤通入过量的二氧化碳
⑥加入足量的NaOH溶液 ⑦加入足量的FeCl3溶液 ⑧加入乙酸与浓硫酸混合液加热。
合理的实验操作步骤及顺序是
| A.④⑤③ | B.⑥①⑤③ | C.⑧①⑦ | D.⑧②⑤③ |
设NA为阿伏加德罗常数,下列叙述中正确的是
| A.pH=1的甲酸溶液中,HCOO-和H+数目之和为0.1 NA |
| B.标准状况下,3.36L乙烯中含有的非极性键数为0.3NA |
| C.1 mol甲基(-CH3)所含电子数10NA |
D.1mol 含有的双键数目约为5×6.02×1023 含有的双键数目约为5×6.02×1023 |