NA代表阿伏加德罗常数。下列有关叙述正确的是
| A.常温下,分子数为NA的CO、C2H4混合气体的质量为28 g,体积可能为22.4L |
B.2.4g金属镁与足量的盐酸反应,转移电子数为2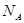 |
| C.标准状况下,2.24LH2O含有的分子数等于0.1NA |
D.34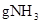 中含N—H键数目为3 NA 中含N—H键数目为3 NA |
钢铁暴露在潮湿的空气中会发生析氢腐蚀或吸氧腐蚀,发生吸氧腐蚀时正极反应式为 ()
| A.4H++ 4e-= 2H2↑ | B.2H2O+O2+ 4e一 =4OH- |
| C.2Fe一 4e- =2Fe2+ | D.4OH一—4e一=2H2O+O2↑ |
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1·S-1
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1·S-1
②用物质 B 表示的反应的平均速率为 0.6 mol·L-1·S-1
③ 2 s 时物质 A 的转化率为70%
④ 2 s 时物质 B 的浓度为 0.7 mol·L-1,其中正确的是()
| A.①③ | B.①④ | C.②③ | D.③④ |
用惰性电极电解下列溶液,一段时间后,再加入一定量的另一种物质(括号内),溶液能与原来溶液完全一样的是()
| A.CuCl2 [CuSO4] | B.NaOH [NaOH] |
| C.NaCl [HCl] | D.CuSO4 [Cu(OH)2] |
把分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为()
| A.1︰2︰3 | B.3︰2︰1 | C.6︰3︰1 | D.6︰3︰2 |
在一定条件下,对于A2(g)+3B2(g) 2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最快的是
2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最快的是 ( )
( )
| A.v(A2)=0.8 mol·L-1·s-1 | B.v(A2)=30 mol·L-1·min-1 |
C.v(AB3)=1.0 mol ·L-1·s-1 ·L-1·s-1 |
D.v(B2)=1.2 mol·L-1·s-1 |