根据下表信息,判断以下叙述正确的是部分短 周期元素的原子半径及主要化合价
周期元素的原子半径及主要化合价
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
| A.氢化物的沸点为HnT<HnQ |
| B.L、R的单质与稀盐酸反应的速率为R>L |
| C.M与T形成的化合物具有两性 |
| D.L、Q形成的简单离子的核外电子数相等 |
下列叙述正确的是
| A.浓盐酸具有强化性能将铜等不活泼金属氧化 |
| B.稀硝酸与活泼金属反应主要放出氢气,而浓硝酸则使金属钝化 |
| C.浓硝酸、稀硝酸和浓硫酸都是强氧化剂 |
| D.在室温下,铜既可与浓硝酸反应,也可与浓硫酸反应 |
设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是
| A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢 |
| B.分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少 |
| C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成 |
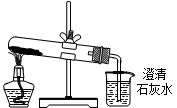
| D.分别将等量的白色粉末用下图装置进行实验,比较澄清石灰水是否变混浊 |
下列现象因发生取代反应而产生的是
| A.甲烷与氯气混合,光照一段时间后黄绿色消失 |
| B.将苯加入溴水中,振荡后水层接近无色 |
| C.乙烯使溴的四氯化碳溶液褪色 |
| D.乙烯使酸性高锰酸钾溶液褪色 |
分子为C5H12的有机物的同分异构体的数目为
| A.2 | B.3 | C.4 | D.5 |
下列物质的变化,不能通过一步化学反应完成的是
| A.NO2→HNO3 | B.Cl2→HClO | C.SiO2→H2SiO3 | D.H2SO4(浓)→SO2 |