“封管实验”具有简易、方便、节约、绿色等优点。观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是
| A.加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色固体 |
| C.加热时,c中溶液红色变深,冷却后又逐渐变浅 |
D.水浴时,d内气体颜色变浅,e内气体颜色变浅(2NO2 N2O4ΔH<0) N2O4ΔH<0) |
应2X(g)+Y(g) 2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
| A.T1<T2,P1<P2 | B.T1<T2,P1>P2 | C.T1>T2,P1>P2 | D.T1>T2,P1<P2 |
在一定温度下,反应1/2H2(g)+ 1/2X2(g) 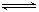 HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
| A.5% | B.17% | C.25% | D.33% |
一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g)+Y(g) 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
| A.用X表示此反应的反应速率是(0.1—0.2a)mol·(L·min)-1 |
| B.当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
| C.向平衡后的体系中加入l mol M,平衡向逆反应方向移动 |
| D.向上述平衡体系中再充入l mol X,v(正)增大,v(逆)减小,平衡正向移动 |
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是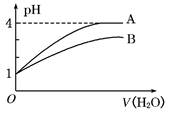
| A.A酸比B酸的电离程度小 |
| B.B酸比A酸容易电离 |
| C.A是强碱,B是弱碱 |
| D.pH=1时,B酸的物质的量浓度比A酸大 |
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
B.溶液中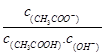 不变 不变 |
| C.醋酸的电离程度增大,C(H+)亦增大 |
| D.再加入10mlpH=11的NaOH溶液,混合液pH=7 |