X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各
元素中电负性最大。请回答下列问题:
(1) X、Y的元素符号依次为 (1分)、 (1分);
(2) XZ2与YZ2分子的立体结构分别是V形(1分)和直线形(1分),相同条件下两者在水中的溶解度较大的是 (1分)(写分子式)’理由是因为 (2分);
(3) Q的元素符号是 (1分),它属于 周期,它的核外电子排布式为 (1分),在形成化合物时它的最髙化合价为 (1分);
(4) 用氢键表示式写出£的氢化物溶液中存在的所有氢键 (4 分)。
铁氧体是一类磁性材料,通式为MO·xFe2O3(M为二价金属离子),如Fe3O4可表示为FeO·Fe2O3,制备流程为: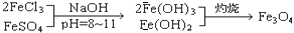
根据题意回答:
(1)现称取2.8 g铁粉,加入一定量的稀硫酸使其完全溶解后,再加入g的FeCl3固体,经上述反应后,方可得到纯净的Fe3O4;
(2)如果以MgSO4和FeCl3为原料,要获得18.0克MgO·2Fe2O3,在制取过程中至少需要1 mol/L的NaOH溶液mL;
(3)在一次制备Fe3O4的实验中,由于反应物比例控制不当,获得了另一种产品。取一定量该产品溶于足量盐酸中,还需通入标准状况下672 mLCl2才能把溶液中的Fe2+全部氧化为Fe3+,然后把所得溶液蒸干,灼烧至恒重,得9.6 g固体。该产品的化学式为;
(4)有一种在电子工业上应用广泛的含铬铁氧体,其组成可表示为: ,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为。
,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为。
下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,D是应用最广泛的金属。根据图示回答问题: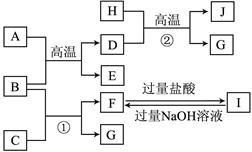
(1)反应②的化学方程式是;
(2)J与氢碘酸反应的离子方程式是;
(3)要使溶液F中的一种金属元素全部以沉淀的形式析出,最适宜加入的反应物是(填化学式);I→F的离子方程式为。
(1)完成并配平白磷和氯酸溶液反应的化学方程式:
P4 + HClO3 + → HCl + H3PO4
(2)白磷有毒,在实验室可采用CuSO4溶液进行处理,其反应为:
11P4 + 60CuSO4 + 96H2O → 20Cu3P + 24H3PO4 + 60H2SO4
该反应的氧化产物是,若有1.1 mol P4反应,则有mol电子转移;
(3)磷的一种化合物叫亚磷酸(H3PO3)。
已知:⑴0.1 mol/L H3PO3溶液的pH = 1.7;
⑵H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;⑶H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。关于H3PO3的说法:①强酸;②弱酸;
③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是。
| A.②④⑥ | B.②③⑥ | C.①④⑤ | D.②③⑤ |
A为两种固体的混合物,G和I为溶液D的组成成分,E为红褐色沉淀,J为淡黄色固体。反应所加的试剂均足量。
(1)混合物A一定含有的元素为(写元素符号);
(2)溶液F一定含有的阴离子为(写离子符号);
(3)写出B+G―→J的化学方程式:
写出溶液C―→溶液D的离子方程式:;
(4)I溶液I中溶质的阳离子常作净水剂,其作用原理是(用离子方程式表示):
。
(8分)有一无色透明澄清溶液,可能含有较大量的Cu2+、Ba2+、SO、NO、
I-、S2-、H+、K+等离子中两种或多种,做如下实验:
①取溶液少量加入铁粉有气体放出;
②另取原溶液加Na2SO3溶液后有气体放出,也有白色沉淀生成,再加盐酸沉淀不完全消失;
③另取原溶液加入AgNO3溶液无沉淀生成。
(1)由此判断原溶液中一定含有的离子是,一定不含有的离子是,可能含有的离子是;
(2)有关反应①的离子方程式为。