用NA表示阿伏加德罗常数。下列叙述正确的是 ( )
| A.2.0 g重水(2H2O)中含有的质子数为1.0 NA |
| B.在电解食盐水的实验中,测得则阴极析出的气体的分子数为0.5NA,则电解后溶液的pH为14。 |
| C.25℃时,1 L pH=14的氢氧化钠溶液中约含有6.02×l023个氢氧化钠分子 |
| D.1mol白磷分子中所含共价键数为4NA |
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量之比为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为( )
| A.1∶5 | B.2∶9 | C.1∶7 | D.1∶9 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液200 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中( )
| A.至少存在5种离子 |
| B.SO42-、NH4+、Fe3+一定存在, Cl-可能不存在 |
| C.Cl-一定存在,且c(Cl-) ≥ 0.2mol/L |
| D.CO32-、Al3+一定不存在,K+可能存在 |
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为()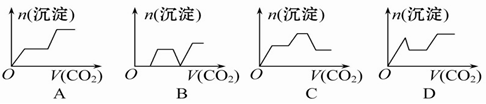
下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )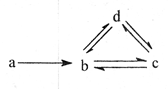
| a |
b |
c |
d |
|
| ① |
Si |
SiO2 |
H2SiO3 |
Na2SiO3 |
| ② |
N2 |
NO |
NO2 |
HNO3 |
| ③ |
Cu |
CuO |
Cu(OH)2 |
CuSO4 |
| ④ |
Na |
NaOH |
Na2CO3 |
NaHCO3 |
A.①② B.②③ C.③④ D.②④
下列表示对应化学反应的离子方程式正确的是()
| A.向醋酸钠水溶液中通入少量CO22CH3COO— + CO2+H2O = 2CH3COOH + CO32— |
| B.向FeBr2溶液中通过量的Cl2:2Fe2++2Br-+2Cl2= 2Fe3++4Cl-+Br2 |
| C.将铝片放入少量NaOH溶液中2Al+2OH-+2H2O =2AlO2-+3H2↑ |
| D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: |
2MnO4-+ 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O