T℃时,有甲.乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲.乙两容器中加入6mol A和3mol B,发生反应如下:
3A(g)+b B(g) 3C(g)+2D(g),(b为
3C(g)+2D(g),(b为 3的正整数) 。
3的正整数) 。
4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;
t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。
根据题给的信息回答下列问题:
(1)甲容器中反应的平均速率 (B)= 。
(B)= 。
(2)在温度T℃时,该反应的化学平衡常数为__________________.
由下表数据可知该反应为______________(填“吸热”“放热”)反应。
化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(3)T℃时,在另一个体积与乙相同的丙容器中,为了达到平衡时B的浓度仍然为0.8mol/L,起始时,向丙容器中加入C、D的物质的量分别为3mol.2mol,则还需加入A.B的物质的量分别是___________.___________。
已知CuSO4溶液分别与Na2CO3、Na2S溶液的反应情况如下:
| CuSO4 +Na2CO3 |
主要: Cu2+ + CO32- + H2O = Cu(OH)2↓ + CO2↑ |
| 次要: Cu2+ + CO32-= CuCO3↓(几乎不发生反应) |
|
| CuSO4 +Na2S |
主要: Cu2+ + S2- =" " CuS↓ |
| 次要: Cu2+ + S2- + 2H2O = Cu(OH)2↓ + H2S↑(几乎不发生反应) |
据此判断,下列几种物质Ksp大小的比较中正确的是
A.CuS <Cu(OH)2<CuCO3 B.Cu(OH)2<CuS< CuCO3
C.CuCO3<Cu(OH)2<CuS D.CuCO3< CuS < Cu(OH)2
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法错误的是
| A.电池放电时Na+从a极区移向b极区 |
| B.每消耗3mol H2O2,转移的电子为3mol |
| C.该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |
| D.电极b采用MnO2,MnO2既作电极材料又有催化作用 |
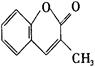
3-甲基香豆素有香草味,可用于香料及化妆品,其结构简式见图。关于它
|
的说法正确的是
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
| A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
下列离子方程式书写正确的是
①等体积等物质的量浓度的氢氧化钡稀溶液与碳酸氢铵稀溶液混合
Ba2+ + 2OH – + NH4+ + HCO3 – = BaCO3↓+ NH3·H2O + H2O
②氯化铝溶液中加入过量的氨水 Al3+ + 4NH3·H2O = 4NH4+ + AlO2 – + 2H2O
③把Fe(OH)2固体投入到稀HNO3中:Fe(OH)2+2H+=Fe2++2H2O
④硫酸铝铵[NH4Al(SO4)2]溶液中滴加Ba(OH)2溶液并加热,刚好使NH4+全部转化为NH3:NH4++Al3++2SO42-+2Ba2++4OH-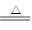 NH3↑+Al(OH)3↓+2BaSO4↓+H2O
NH3↑+Al(OH)3↓+2BaSO4↓+H2O
⑤过氧化钠固体与水反应:2O22‾+2H2O=4OH‾+O2↑
⑥氨水中通入过量二氧化硫:2NH3•H2O + SO2 = 2NH4+ +SO32‾ +H2O
| A.①③ | B.①④ | C.①⑥ | D.②④⑤ |