某学生欲用已知物质的量浓度的HCl测定未知浓度的NaOH溶液,将HCl置于滴定管,氢氧化钠溶液置于锥形瓶,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定未知浓度的NaOH溶液,滴定到终点时锥形瓶中颜色变化为 。
(2)下列操作中可能无法会怎样影响所测NaOH溶液浓度(填偏大.偏小或不影响)
A.酸式滴定管未用标准浓度的HCl润洗就直接注入标准盐酸
B.读数时,开始平视,结束时俯视 液面
液面
(3)某学生根据3次实验记录有关数据如下:
| 滴定次数 |
待测NaOH溶液体积(mL) |
0.1000mol/L HCl溶液的体积(mL) |
|
| 滴定前刻度 |
滴定后刻度 |
||
| 第一次 |
25.00 |
0.00 |
26.11 |
| 第二次 |
25.00 |
1.56 |
30.30 |
| 第三次 |
25.00 |
0.22 |
26.31 |
请选择合理的数据计算NaOH溶液的物质的量浓度:c(NaOH)=________________。
实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律摆放在实验桌上,如下图所示。做“硫酸的性质”的实验时,某同学取用Ba SO4溶液后,应把它放回的位置是
下列物质中,属于芳香烃且属于苯的同系物的是()
A. |
B.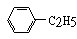 |
C.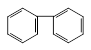 |
D.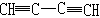 |
下列实验操作错误的是( )
| A.分夜时,分夜漏斗中下层溶液从下口放出、上层溶液从上口到出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.可用酒精萃取碘水中的碘 |
| D.称量时,称量物一般放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
相同碳原子数的烷烃、烯烃、炔烃,在空气中完全燃烧生成二氧化碳和水,需要空气量的比较中正确是()
| A.烷烃最多 | B.烯烃最多 | C.炔烃最多 | D.三者一样多 |
下列烷烃的一氯取代物中没有同分异构体的是()
| A.丙烷 | B.丁烷 | C.异丁烷 | D.新戊烷 |