据媒体报道:以氢氧燃料电池为动力的公交车即将在北京试运行。质子交换膜燃料电池 (PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂为电极,导电离子是H+。下列对该燃料电 池
池 的描述正确的是
的描述正确的是
①正极反应为:O2+4H++4e—= 2H2O ②电子由负极流向正极
③总的化学反应为:2H2+O2===2H2O ④氢离子通过电解质向正极移动
A.①②③ B.②③④ C.①②④ D.①②③④
己烯雌酚是一种激素类药物,结构如右图所示,下列有关叙述中正确的是
| A.分子中有7个碳碳双键,可以与氢气1:7加成 |
| B.该分子中有2个H,2个O,6个C共直线 |
| C.该分子对称性好,所以没有顺反异构 |
| D.该有机物分子中,最多可能有18个碳原子共平面 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是
某烯烃与H2加成后的产物是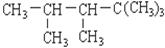 ,则该烯烃的结构式可能有
,则该烯烃的结构式可能有
| A.1种 | B.2种 | C.3种 | D.4 种 |
烃分子中若含有双键、三键或环,其碳原子所结合的氢原子数则少于碳原子数对应烷烃所含有的氢原子数,亦具有一定的不饱和度(用Ω表示)。下表列出几种烃的不饱和度:
| 有机物 |
乙烯 |
乙炔 |
环己烷 |
苯 |
| Ω |
1 |
2 |
1 |
4 |
据此下列说法不正确的是:
A.1mol Ω=3的不饱和链烃再结合3mol H2,即达到饱和
B.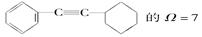
C.C4H8的不饱和度与C3H6、C2H4的不饱和度不一定相同
D.CH3CH2CH=CH2与环丁烷的不饱和度相同
1体积某气态烃只能与1体积氯化氢气体发生加成反应,生成氯代烷。1mol此氯代烷可与7mol氯气发生完全的取代反应,则该烃的结构简式为:
| A.CH3CH=CH2 | B.CH2=CH2 | C.CH≡C—CH3 | D.CH3CH2CH=CH2 |