门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是
| A.X单质不易与水反应 | B.XO2可被碳或氢还原为X |
C.XCl4的沸点比SiCl4的高 | D.XH4的稳定性比SiH4的高 |
若NA表示阿伏加德罗常数,下列说法正确的是()
| A.含有NA个氖原子的氖气在标准状况下的体积约为11.2L |
| B.2.3gNa被O2完全氧化时,失去电子数为0.1NA。 |
| C.2Llmol·L-1的盐酸中所含氯化氢分子数约为2NA |
| D.标准状况下,5.6LCCl4含有的分子数为0.25NA |
将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是 ( )Ⅰ
| A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠 |
| B.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液 |
| C.最后变成碳酸钠粉末 |
| D.该过程的所有化学反应均为氧化还原反应 |
钢铁在潮湿的空气中会形成原电池而被腐蚀,下列说法正确的是()
A.原电池的正极反应为:O2+2H2O+ 4e-→4OH- 4e-→4OH- |
| B.原电池的负极反应为:Fe→Fe3++3e- |
| C.钢铁设备上连接铜块可以防止腐蚀 |
| D.钢铁与外加直流电源的正极相连可以防止腐蚀 |
为预防“H1N1”甲型流感,同学们每天用“84”消毒液(NaClO溶液)消毒,下列说法正确的是
| A.NaClO溶液的消毒原理是使蛋白质变性 |
| B.1molCl2与足量NaOH溶液反应转移2mol电子 |
| C.NaClO溶液的漂白原理与Na2O2、SO2相同 |
| D.“84”消毒液与“洁厕灵”(盐酸)共同使用,可达到既清洁又消毒的双重效果 |
下列选项中正确的是
| A.1L0.5mol·L-1稀硫酸与1L1mol·L-1氢氧化钠溶液反应放出57.3kJ的热量: H2SO4(aq) +2Na  OH(aq) = Na2SO4(aq) +2H2O(1);△ H = -57.3 kJ· mol-1 OH(aq) = Na2SO4(aq) +2H2O(1);△ H = -57.3 kJ· mol-1 |
B.某酸的酸式盐NaHY水溶液显碱性,则H2Y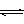 2H++Y2— 2H++Y2— |
C.纯碱溶液显碱性的原因用离子方程式可表示为:CO32—+2H2O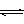 H2CO3+2OH— H2CO3+2OH— |
D.以惰性电极电解KCl溶液的离子方程式为:2Cl-+2H2O  H2↑+2OH-+Cl2↑ H2↑+2OH-+Cl2↑ |