用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.46gNO2和N2O4的混合物中含有的原子总数一定是3NA |
B.500℃、30MPa下:N2(g)+3H2(g)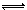 2NH3(g)△H=-38.6kJ·mol-1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ 2NH3(g)△H=-38.6kJ·mol-1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ |
| C.标准状况下,11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为NA |
| D.1 mol SiO2晶体中,Si-O键的数目为2NA |
常温下,向一定浓度的醋酸溶液中逐滴加入氢氧化钠溶液直至过量,在此操作过程中,有关溶液中离子浓度变化的大小关系不正确的是()
| A.当pH=7时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
| B.当pH>7时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.当恰好完全中和时,c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.反应全程都有关系:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
下列图象能表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)()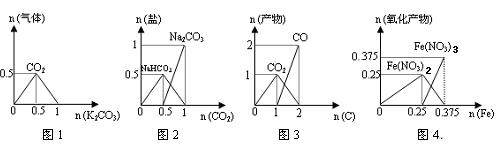
| A.图1:n(HCl)=1mol,K2CO3加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
海南的毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示:对该化合物的叙述正确的是()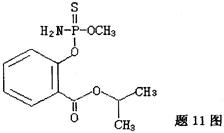
| A.该化合物属于芳香烃 |
| B.该化合物的分子式为C11H14O4NPS |
| C.该化合物能发生加聚反应、水解反应和酯化反应 |
| D.该化合物中至少有7个碳原子在同一平面 |
下列各组离子在指定溶液中,能大量共存的是()
| A.强碱性溶液中:K+,ClO-,Ba2+,Cl- |
| B.水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-,CO32-,NO3-,NH4+ |
| C.使甲基橙变红的溶液中:Fe2+,MnO4-,NO3-,Na+ |
| D.中性溶液中:Al3+,NO3-,Cl-,S2- |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是()
①12.4g白磷晶体中含有的P-P键数约是0.6 NA
②电解精炼铜时转移了NA个电子,阳极溶解32 g铜
③7.8 g Na2S和Na2O2的固体混合物中含有的阴离子数大于0.1 NA
④CO(g)的燃烧热是283.0kJ /mol,则2CO2(g)
/mol,则2CO2(g)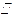 2CO(g)+O2(g)△H=+2×283.0kJ/mol
2CO(g)+O2(g)△H=+2×283.0kJ/mol
⑤2.9g 2CaSO4·H2O含有的结晶水分子数为0.02 NA
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
⑦含0.1mol溶质Na2CO3的溶液中,所含阴离子总数大于0.1NA
| A.①④⑤⑦ | B.①④⑦ | C.①③④⑤⑥ | D.②③⑤⑥ |