2009年12月7日~18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议。而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:某温度下,在容积为2L的密闭容器中,充入1mol CO2和3.25mol H2,在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间变化如右图所示: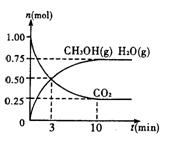
① 从反应开始到平衡,氢气的平均反应速 (H2)=_______。
(H2)=_______。
②下列措施中一定不能使 (CH3OH)/ (CO2)增大的是_____。
(CH3OH)/ (CO2)增大的是_____。
| A.降低温度 | B.缩小容器的容积 |
| C.将水蒸气从体系中分离 | D.使用更有效的催化剂 |
(2)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的电离平衡常数K=___________。(已知:10-5.6=2.5×10-6)。
HCO3-+H+的电离平衡常数K=___________。(已知:10-5.6=2.5×10-6)。
(3)标准状况下,将1.12L CO2通入100mL 1mol·L-1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为
________________;
(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处的通入的是_____________(填“乙醇”或“氧气”),b处电极上发生的电极反应是___________
__________________________________________。
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为_______。
据新闻媒体报道,误食亚硝酸钠已造成多起人畜中毒事件,因为它外观类似食盐又有像食盐一样的咸味。亚硝酸钠能引起人体中毒。已知亚硝酸钠能发生如下反应:
NaNO2+HI——NO↑+I2+NaI+H2O
(1)上述反应中,氧化剂是__________,若有0.05 mol还原剂被氧化,则被还原的氧化剂是____________mol。
(2)根据上述反应,可以用试纸和一些生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐。可供选用的物质有:①自来水,②碘化钾淀粉试纸,③淀粉,④白糖,⑤食醋,⑥白酒。进行实验时,必须使用的物质有(填编号)____________。
(3)某厂废切削液中有2%—5%NaNO2,直接排放会造成环境污染,在下列试剂中:①NaCl,②NH4Cl,③H2O2④浓H2SO4,能使NaNO2转化为不引起二次污染的N2的是(填编号)_________,化学方程式为___________________________________________。
已知1 mol CuSCN在下列反应中失去7 mol电子,完成并配平下列化学反应方程式:CuSCN+KMnO4+H2SO4——HCN+CuSO4+MnSO4+K2SO4+H2O
已知氧化还原反应:NaNO2+NH4Cl——NaCl+H2O+N2↑,若得到m mol的N2,则电子转移数为__________个,此时氧化产物与还原产物的质量之比为____________。
对于CO中毒、心肌梗塞、冠心病或小儿肺炎等危重患者都要采用吸氧治疗。普通医务室中没有氧气瓶,但一般都有消毒用的30%的过氧化氢溶液。同时还有可选用的试剂:KMnO4、HCl、H2SO4、MnO2、Mg粉、CuSO4、NaCl、葡萄糖。请写出一种能使过氧化氢中氧完全释放出来的反应方程式:_____________________________________________。
有两份铜屑,将它们分别与足量的浓H2SO4和稀HNO3完全反应。若放出的气体在常温常压下体积相同,则这两份铜屑的质量比是________。