下列对于溶液中的问题叙述正确的是
| A.向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 |
| B.对于水的电离而言,加入强酸、强碱会促进水电离,而加入弱酸、弱碱则会抑制水电离 |
| C.5mL 0.02mol/L HCl溶液与5mL 0.02mol/L Ba(OH)2溶液混合,经充分反应后,如果溶液体积为10mL,则溶液的pH=12 |
| D.常温下,将稀NaOH溶液与CH3COOH溶液混合,可能出现pH>7,且c(OH—)>c(Na+)>c(H+)>c(CH3COO—)的情况 |
β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。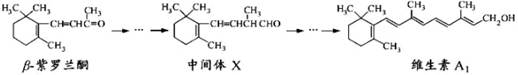
下列说法正确的是
| A.β—紫罗兰酮可使酸性KMnO4溶液褪色 | B.1mol中间体X最多能与2molH2发生 加成反应 加成反应 |
| C.维生素A1易溶于NaOH溶液 | D.β—紫罗兰酮与中间体X互为同分异构体 |
下列有机物命名正确的是
A.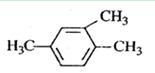 1,3,4-三甲苯 1,3,4-三甲苯 |
B.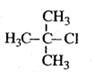 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 |
C.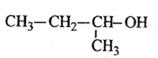 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D.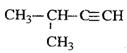 2-甲基-3-丁炔 2-甲基-3-丁炔 |
下列说法正确的是
| A.纤维素和淀粉遇碘水均显蓝色 | B.蛋白质、乙酸和葡萄糖均属电解质 |
| C.溴乙烷与NaOH乙醇溶液共热生成乙烯 [ | D. 乙酸乙酯和食用植物油均可水解生成乙醇 乙酸乙酯和食用植物油均可水解生成乙醇 |
某有机物与过量的金属钠反应,得气体VA L ,另一份等质量的该有机物与纯碱反应,得气体VB L(同温同压)。若VB ≠0且VA>VB ,则有机物是
| A.CH3COOH | B.HOOC CH2 CH (OH)COOH |
| C.HOOC—COOH | D.HO—CH2-CH2-OH |
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2 CH3CHBrCH2Br②CH3CH2OH
CH3CHBrCH2Br②CH3CH2OH  CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O④C6H6+HNO3
CH3COOCH2CH3+H2O④C6H6+HNO3 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |