将有机化合物的分子式或结构简式变形书写,在分析问题的过程会取得意想不到的好效果。已知甲酸(HCOOH)与浓硫酸混合在50——60℃时,会发生脱水生成CO;乙醇(CH3CH2OH)与浓硫酸混合在170℃时脱水生成乙烯(C2H4或CH2=CH2),则草酸HOOC—COOH与浓硫酸在一定温度下脱水会生成
| A.CO | B.CO2 | C.CO和 CO2 | D.C2O3 |
A、B、C、D、E五种短周期元素,原子序数依次递增,A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,而E在同周期元素中原子半径最小。A、C、D三种元素可形成化合物甲,B、C、D三种元素可形成化合物乙,甲和乙均为中学化学常见物质。请回答:
(1)甲的电子式为,其中所含化学键类型为。
(2)A的单质与C的单质在碱性条件下构成燃料电池,其正极反应式为;负极反应式为。
(3)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH—的物质的量浓度c(OH—)甲:c(OH—)乙=.
(4)A与C、D与C可形成化合物A2C、A2C2、D2C、D2C2,说出的一种用途;
写出A2C2与E的单质反应的化学方程式。
(5)浓氨水与固体甲混合,可用于快速制取少量氨气,其原因是
(请用必要的方程式和简要的文字加以说明)。
1951年有人从煤矿的坑水中分离出了一种氧化铁硫杆菌。它能促使促使黄铁矿(FeS2)氧化成硫酸铁和硫酸。后来又发现了能把矿物中的硫或硫化物氧化成硫酸的氧化硫杆菌。而硫酸和硫酸铁能将某些矿石中金属元素转化成相应金属的的硫酸盐。从而开辟了“细菌冶金”的先河。氧化铁硫杆菌的活动过程如图:其中a过程发生的反应为:4FeS2+15O2+2H2O 2Fe2(SO4)3+2H2SO4。
2Fe2(SO4)3+2H2SO4。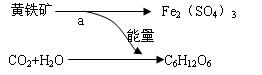
则下列说法不正确的是
| A.a过程是释放能量的过程 |
| B.b过程类似于植物的光合作用,细菌将能量储存在C6H12O6中 |
| C.细菌在反应a过程中起了催化剂的作用 |
| D.有些细菌可以直接把含重金属的矿石溶解,得到含重金属离子的溶液 |
下列金属或氧化物可以完全溶解的是
| A.1molZn与含1molHCl的稀盐酸共热 |
| B.1molCu与含2molH2SO4的浓硫酸共热 |
| C.1molCu与含4molHNO3的浓硝酸 |
| D.1molMnO2与含4molHCl的浓盐酸共热 |
已知次氯酸和次氟酸的分子结构相似,分子中所有原子都形成了稳定结构。下列说法不正确的是
| A.次氯酸的结构式为H—O—Cl |
| B.严格说来,次氯酸的分子应写为HOCl |
| C.次氟酸应具有很强的氧化性 |
| D.次氟酸中氧元素的化合价为+1价 |