在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
⑴已知:N2(g)+ O2(g)="2NO(g)" △H=+180.5 kJ/mol
2C(s)+ O2( g)="2CO(g)" △H="-221.0" kJ/mol
g)="2CO(g)" △H="-221.0" kJ/mol
C(s)+ O2(g)=CO2(g) △H="-393.5" kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H= ▲ 。
⑵某研究性学习小组在技术人员的指导下,按下列流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。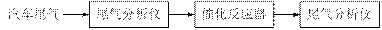
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、 ▲ 等必须相同。
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。
⑶CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。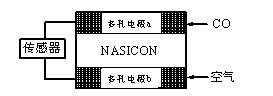
下列说法错误的是 ▲ 。
A.负极的电极反应式为 :CO+O2—―2e-=CO2 :CO+O2—―2e-=CO2 |
| B.工作时电极b作正极,O2-由电极a流向电极b |
C.工作 时电子由电极a通过传感器流向电极b 时电子由电极a通过传感器流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
已知M2+离子3d轨道上有5个电子,则
(1)M原子的外围电子排布图(轨道表示式)为:。
(2)M原子的最外层电子数为个;最高能级中电子数为个。
(3)M元素在周期表中的位置是:。
已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。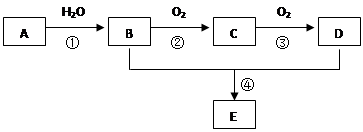
请回答下列问题:
(1)写出A的结构简式 。
(2)B、D分子中的官能团名称分别是 , 。
(3)物质B可以被直接氧化为D,需要加入的试剂是。
(4)写出下列反应的化学方程式:
①;反应类型:。
④;反应类型:。
现有短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和为5。X元素原子最外层上的电子数是Y元素原子最外层与Z元素原子最外层电子数之和;Y元素最外层上电子数是其电子层数的2倍,X和Z可以形成XZ3型化合物,请回答问题:
(1) X的名称_________,Y的名称_________,Z的名称_________。
(2) XZ3的化学式为________,电子式为______,分子间存在________键。
(3)X最高价氧化物对应水化物的浓溶液与红热的Y单质反应的化学方程式为____________________________。
在2升容器中加入18g水蒸气,28g一氧化碳,在t℃时(t>100),发生如下反应:
CO+H2O CO2+H2,在最初5秒钟内,一氧化碳的平均反应速率是0.02 mol·l-1·s-1求:
CO2+H2,在最初5秒钟内,一氧化碳的平均反应速率是0.02 mol·l-1·s-1求:
(1) 5秒钟末,容器内CO2和H2O蒸汽浓度分别为________,__________。
(2) 若设计此反应为一个原电池,则负极发生________反应(填“氧化”,“还原”),负极消耗的物质化学式为____________。
有两种气体单质Am和Bn,已知2.4克Am和2.1克Bn所含有的原子个数相同,分子个数比为2:3;又知A和B的原子核内质子数都等于中子数,且A原子中的L层电子数是其K层电子数的3倍,则A元素的元素符号为________,B元素的元素符号为_________,m=_________;A和B形成红棕色化合物化学式为_________。