只用一种试剂即可鉴别 (NH4)2SO4、NH4Cl、AlCl3、Na2SO4、NaCl五种溶液(可选择加热),这种试剂是
| A.NaOH | B.HCl | C.Ba(OH)2 | D.H2SO4 |
从实验安全角度考虑,下列操作错误的是()
| A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗 |
| C.若苯酚溶液沾到皮肤上,应立即用大量水冲洗 |
| D.配制浓硫酸和乙醇混合液时,先将浓硫注入烧杯中,然后,边加无水酒精边用玻璃棒搅拌至冷却 |
下列实验装置设计正确,且能达到目的的是: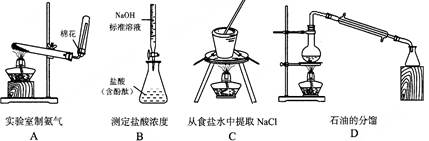
向含1mol HCl和1mol MgSO4的混合溶液中加入1mol·L—1的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图正确的是()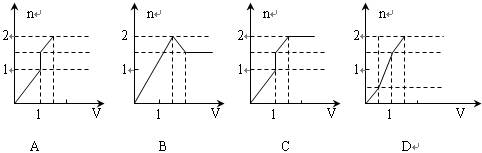
某溶液中只可能含有下列离子中的几种(不考虑溶液中较少的H+和OH-)Na+、NH4+、SO42-、CO32-、NO3-。取200mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL。实验2:第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33g。下列说法正确的是()
| A.该溶液中可能含有Na+ | B.该溶液中肯定含有NH4+、S042-、CO32-、NO3- |
| C.该溶液中一定不含NO3- | D.该溶液中一定含Na+,且c(Na+)≥0.1 mol/L |
下列说法正确的是()
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
| A.①③⑤ | B.②④⑥ | C.②③④ | D.①③⑥ |