我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3 nm)恢复了磁性。“钴酞菁”分子的结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中不正确的是
| A.“钴酞菁”分子分散在水中所形成的分散系不具有丁达尔效应 |
| B.“钴酞菁”分子能透过滤纸 |
| C.此项工作可以用来改变分子的某些物理性质 |
| D.此项工作可广泛应用于光电器件、生物技术等方面 |
下列有关物质性质的应用正确的是
| A.浓硫酸有吸水性,可用于干燥氨气和二氧化硫 |
| B.明矾溶于水能形成胶体,可用于自来水的杀菌消毒 |
| C.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 |
| D.金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1 mol·L-1氨水溶液:K+、Na+、NO3-、AlO2- |
| B.0.1 mol·L-1 Fe(NO3)2溶液:H+、Al3+、SO42-、Cl- |
| C.滴入酚酞显红色的溶液:Na+、Mg2+、NO3-、HCO3- |
| D.由水电离出的c(H+)=10-11mol·L-1的溶液:Ca2+、NH4+、Cl-、CO32- |
下列有关化学用语表示正确的是
A.四氯化碳分子球棍模型: |
| B.二氧化硅的分子式:SiO2 |
C.S2-离子结构示意图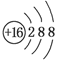 |
D.聚丙烯的结构简式: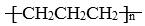 |
据报道,我国于今年进行海域“可然冰”钻探工程,可燃冰分布于深海沉积物或陆域的永久冻土中。“可燃冰”的分子结构模型如图,下列关于“可燃冰”的说法正确的是
| A.可燃冰就是可以燃烧的冰 |
| B.燃烧相同物质的量的可燃冰和甲烷,获得相同的热量 |
| C.水和甲烷均为电解质 |
| D.可燃冰是一种由水分子和甲烷分子形成的有固定组成的化合物 |
有关离子浓度大小比较的判断正确的是
| A.往醋酸中滴加氢氧化钠溶液到溶液呈中性,c(Na+)=c(CH3COO-) |
| B.Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.KHSO3溶液呈酸性,c(K+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) |
| D.0.1mol/L的NH4Cl溶液中,c(NH4+)>c(Cl-)>c(OH-)>c(H+) |