常温下,向25mL0.1mol?L-1 NaOH溶液中逐滴加入0.1mol?L-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是
A.只有在A、B间任一点,溶液中才有:
c(Na+)+c(H+)=c(CH3COO-)+(OH-)
B.在B点,a>25,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=c(Na+)
某合作学习小组讨论辨析以下说法:①冰水混合物和酸雨都是混合物;②水煤气和石油都是可再生能源;③不锈钢和目前流通的硬币都是合金;④稀硫酸和食醋既是化合物又是酸;⑤纯碱和熟石灰都是碱;⑥淀粉溶液和雾都是胶体。上述说法正确的是
| A.③④ | B.③⑥ | C.①③⑤ | D.①③⑥ |
随着社会的发展,人们日益重视环境问题,下列做法或说法不正确的是
| A.将煤液化或气化,获得清洁燃料 |
| B.提倡重拎布袋子、重提菜篮子,重复使用耐用型购物袋 |
| C.对垃圾进行无害化、资源化处理 |
| D.PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 |
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应
Cr2O72–+6Fe2++14H+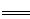 2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
A.阳极反应为Fe-2e- Fe2+ Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.反应过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
在一定温度下,将气体X和气体Y 各0.16 mol充入10 L恒容密闭容器中,发生反应
X(g) + Y(g)  2Z(g)∆H<0,一段时间后达到平衡,反应过程中测定的数据如下表。下列说法正确的是
2Z(g)∆H<0,一段时间后达到平衡,反应过程中测定的数据如下表。下列说法正确的是
| t / min |
2 |
4 |
7 |
9 |
| n(Y)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
A.反应前2min的平均速率v(Z)=2.0×10–5 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
下列表示对应化学反应的离子方程式正确的是
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O =3I 2+6OH- |
B.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.将过量二氧化硫气体通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++3NO3-=Ag++3NO↑+H2O |