有七种物质:①甲烷、②苯、③聚乙烯、④聚异戊二烯、⑤2-丁炔、⑥环己烷、7环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是
| A.③④⑤ | B.④⑤⑦ | C.④⑤ | D.③④⑤⑦ |
下列除去杂质的方法正确的是
| A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
| B.除 CO2中的少量HCl:通入饱和Na2CO3溶液,收集气体 |
| C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
下列有机物的分离提纯方法正确的是
| A.除去乙酸乙酯中含有的乙酸杂质,可以加氢氧化钠溶液充分振荡后,分液。 |
| B.用重结晶的方法分离苯甲酸和氯化钠的混合物 |
| C.将工业酒精直接蒸馏可以获得无水酒精 |
| D.用酸性高锰酸钾溶液可以除掉甲烷中的乙烯杂质。 |
下列有关化学用语表示不正确的是
A.氧的原子结构示意图: |
B.Na2O2的电子式: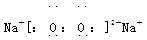 |
| C.HClO的结构式:H—O—Cl | D.中子数为16的硫离子: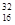 S2- S2- |
图表归纳是学习化学的一种常用方法,某同学如下归纳的下表与右图中对应正确的是
| 选项 |
X |
Y |
Z |
 |
| A |
胶体 |
混合物 |
淀粉溶液 |
|
| B |
化合物 |
酸性氧化物 |
一氧化氮 |
|
| C |
气态氢化物 |
化合物 |
液溴 |
|
| D |
强电解质 |
强酸 |
硫酸 |
下列叙述正确的是
| A.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| B.CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大 |
| C.Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
| D.25℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度 |