下列离子方程式正确的是
A.石灰乳与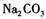 溶液混合: 溶液混合: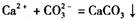 |
B.向沸水中滴加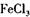 溶液并加热制备 溶液并加热制备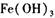 胶体: 胶体: |
C.向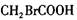 中加;足量的氢氧化钠溶液并加热: 中加;足量的氢氧化钠溶液并加热: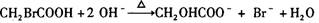 |
D.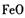 与稀硝酸反应: 与稀硝酸反应: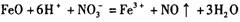 |
下列有关化学用语表示正确的是
| A.乙醛的结构简式:CH3COH |
B.H2O2的电子式: |
C.次氯酸的电子式: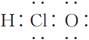 |
D.亚硫酸钠水解的离子方程式:SO32-+2H2O H2SO3+2OH- H2SO3+2OH- |
关于下列各图的叙述,正确的是

A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液的pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
仅用下表提供的仪器和药品,就能达到相应实验目的的是
| 编号 |
仪器 |
药品 |
实验目的 |
| A |
托盘天平(带砝码)、胶头滴管、量筒、烧杯、药匙、玻璃棒 |
NaCl固体、蒸馏水 |
配制一定质量分数的NaCl溶液 |
| B |
分液漏斗、烧瓶、锥形瓶、导管及橡皮塞 |
盐酸、大理石、碳酸钠溶液 |
证明非金属性:Cl>C>Si |
| C |
酸式滴定管、胶头滴管、铁架台(带铁夹) |
已知浓度的盐酸、待测NaOH溶液 |
测定NaOH溶液的物质的量浓度 |
| D |
烧杯、分液漏斗、胶头滴管、铁架台 |
待提纯的AlCl3溶液、NaOH溶液 |
提纯混有MgCl2杂质的AlCl3溶液 |
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验:
| A.步骤Ⅰ中减少的3 g固体一定是混合物 |
| B.步骤Ⅱ中质量减少的物质一定是Cu |
| C.根据步骤Ⅰ、Ⅱ可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2 |
| D.根据上述步骤Ⅱ可以得出m(Fe2O3)∶m(Cu)=1∶1 |
满足分子式为C4H8ClBr的有机物共有
| A.10种 |
| B.11种 |
| C.12种 |
| D.13种 |