下列溶液加入氯化钡溶液生成沉淀,在加入盐酸沉淀消失的是
| A.AgNO3溶液 | B.Na2SO4 溶液 |
| C.Na2SiO3溶液 | D.Na2CO3溶液 |
下列叙述正确的是()
| A.液态HCl不导电,所以HCl是非电解质 |
| B.NH3的水溶液能够导电,所以NH3是电解质 |
| C.液态Cl2不导电,所以Cl2是非电解质 |
| D.BaSO4在熔融状态下能导电,所以BaSO4是电解质 |
氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是()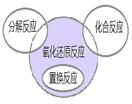
| A.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
B.4NH3 +5O2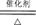 4NO+6H2O 4NO+6H2O |
| C.2NaHCO3=Na2CO3+H2O+CO2↑ |
| D.Cl2+2NaBr=2NaCl+Br2 |
不用其它试剂鉴别①KNO3②Ba(OH)2③MgCl2④CuSO4四种溶液,正确的鉴别顺序是 ( )
| A.①④③② | B.④③①② | C.④②③① | D.②①③④ |
下列实验操作中,错误的是()
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.把几滴FeCl3饱和溶液滴入25mL沸水中制备Fe(OH)3胶体 |
| C.过滤可以除掉粗盐中可溶于水的杂质 |
| D.碘易溶于有机溶剂,可用CCl4萃取碘水中的碘 |
下列各组物质,按化合物、单质、混合物的顺序排列的是()
| A.干冰、铁、氯化氢 | B.生石灰、白磷、熟石灰 |
| C.烧碱、液态氧、碘酒 | D.空气、氮气、胆矾 |