用惰性电极电解100mLCuSO4稀溶液,一段时间内,阴极无气体生成时,在阳极收集到气体56mL(标准状况),若不考虑Cu2+的水解和溶液体积的变化,则此时电解液的pH为
| A.1 | B.0 | C.2 | D.13 |
取c(H+)均为0.5mol/L的盐酸和醋酸各100 mL,分别加水稀释两倍后,再分别加入0.65 g锌粉,相同条件下充分反应,下列说法中,正确的是
| A.将锌反应完所需的时间相同 |
| B.起始时醋酸与锌反应的速率大 |
| C.醋酸与锌反应放出的氢气多 |
| D.两者放出的氢气一样多 |
一定温度下,将1 mol A和1 mol B气体充入2 L恒容密闭容器,发生反应A(g)+B(g)  xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是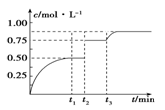
| A.反应方程式中的x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量物质D |
| D.t1~t3间该反应的平衡常数均为4 |
在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g) 2C(g) ΔH<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2C(g) ΔH<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是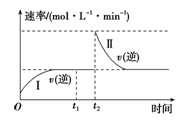
| A.0~t2时,v(正)>v(逆) |
| B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ |
| C.t2时刻改变的条件是向密闭容器中加C |
| D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ |
反应N2O4(g)  2NO2(g)ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g)ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是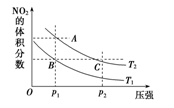
A.A、C两点的反应速率:A>C
B.由状态B到状态A,可以用加热的方法
C.A、C两点混合气体的平均相对分子质量:A>C
D.B、C两点的反应速率:B=C
某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g)  C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
| t/s |
0 |
5 |
15 |
25 |
35 |
| n(A)/mol |
1.0 |
0.85 |
0.81 |
0.80 |
0.80 |
A.反应在前5 s的平均速率v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆)